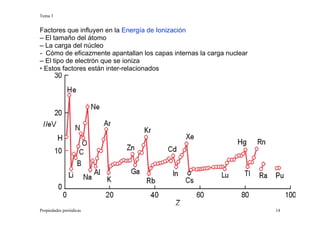
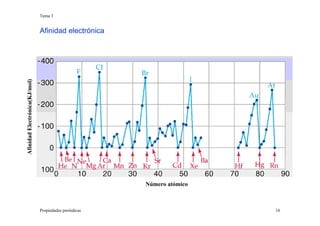
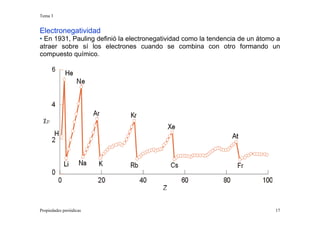
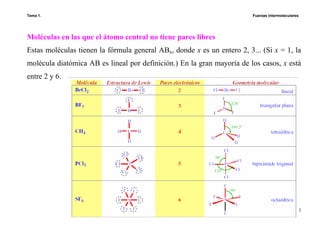
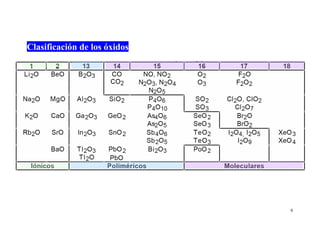
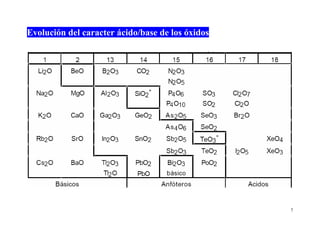
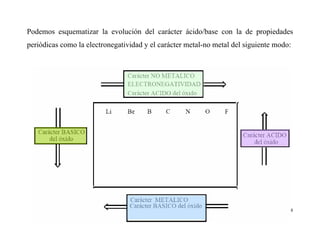
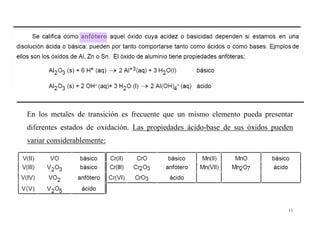
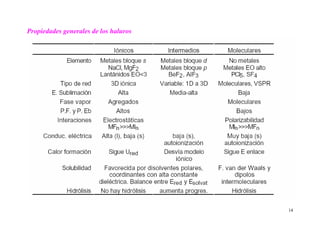
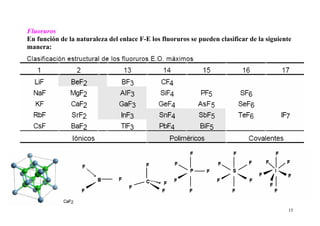
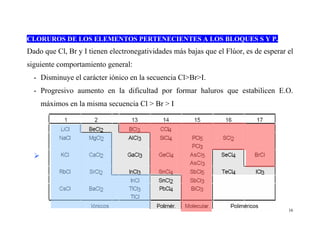
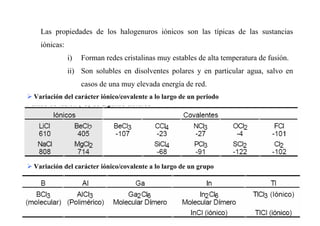
Este documento presenta información sobre las propiedades periódicas de los elementos. Explica la organización de la tabla periódica moderna y las propiedades que se repiten periódicamente como el radio atómico, la energía de ionización y la afinidad electrónica. También describe los factores que influyen en estas propiedades y cómo varían a lo largo de la tabla periódica. Finalmente, introduce el concepto de electronegatividad y su relación con el carácter iónico de los enlaces químicos.