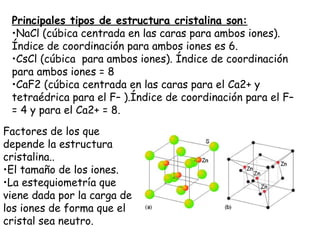
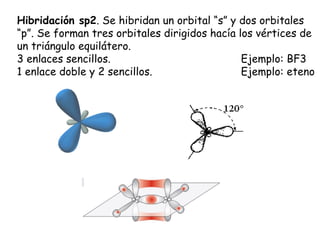
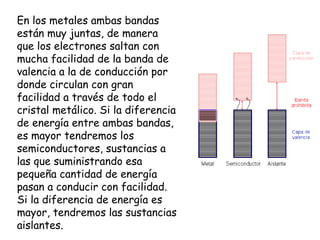
Este documento trata sobre los diferentes tipos de enlaces químicos. Explica que los átomos se unen para alcanzar una situación de mínima energía. Describe los enlaces iónico, covalente y metálico, y las teorías de Lewis y la teoría del enlace de valencia para explicarlos. También analiza las propiedades y estructuras de los compuestos iónicos.