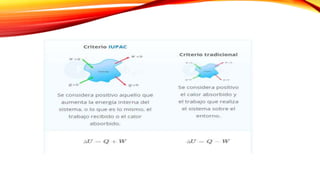
El documento habla sobre la termodinámica y el equilibrio químico. Explica que la termodinámica química estudia la relación entre el calor y el trabajo en reacciones químicas. Luego resume las tres leyes de la termodinámica, incluyendo que la primera ley establece la conservación de la energía, la segunda ley establece que la entropía siempre aumenta, y la tercera ley indica que la entropía llega a cero a temperatura cero.