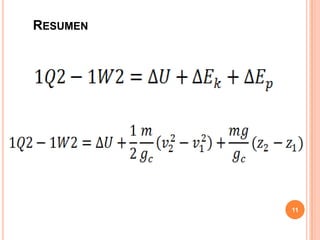Incrustar presentación
Descargado 110 veces








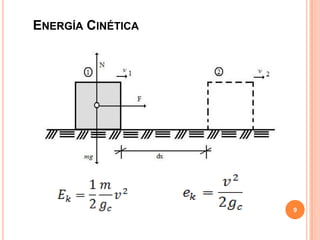
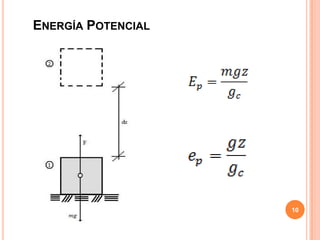
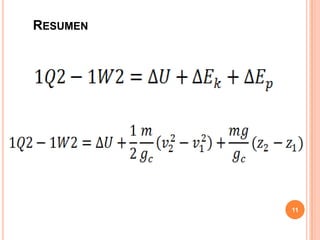

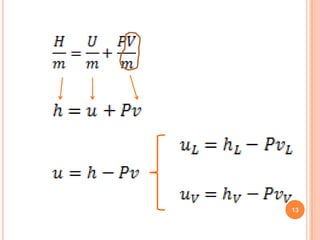

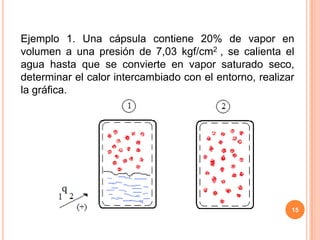

La primera ley de la termodinámica establece que la suma de todos los calores cedidos o recibidos es igual a la suma de todos los trabajos cedidos o recibidos. La energía total de un sistema cerrado depende solo del estado inicial y final y no de la trayectoria, y se designa como E. La energía interna U es la suma de la energía cinética y potencial molecular, mientras que la entalpía H es la suma de U y la presión por el volumen.