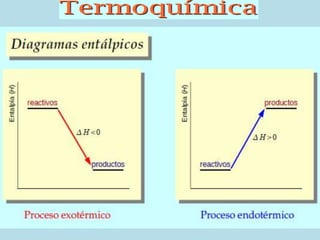
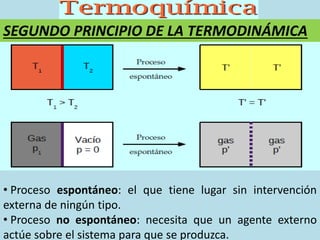
Este documento presenta los conceptos fundamentales de la termoquímica. Explica que la termodinámica estudia los cambios energéticos en todos sus aspectos. Define conceptos clave como sistema, entorno, fase, transformación termodinámica, calor, energía interna, entalpía y procesos termodinámicos. También describe las leyes de la termodinámica, incluyendo la conservación de la energía, y conceptos como entropía y energía libre de Gibbs para determinar la espontaneidad de los proces