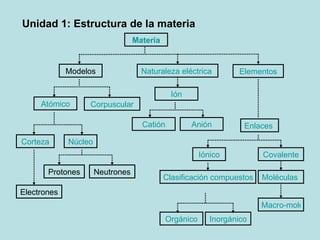
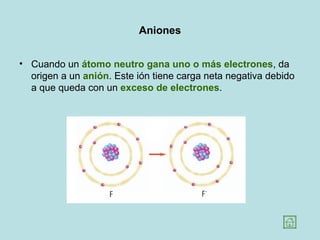
Este documento describe la estructura y composición de la materia a nivel atómico y molecular. Explica que la materia está compuesta de átomos que pueden unirse para formar moléculas e iones. Describe los modelos atómicos históricos y la estructura del átomo con núcleo y electrones. También cubre los tipos de enlaces, moléculas, macromoléculas y la clasificación de compuestos químicos.