Ácidos y bases: clasificación, propiedades y reacciones químicas
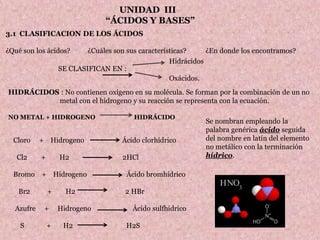
- 1. UNIDAD III “ÁCIDOS Y BASES” 3.1 CLASIFICACION DE LOS ÁCIDOS ¿Qué son los ácidos? ¿Cuáles son sus características? ¿En donde los encontramos? HIDRÁCIDOS : No contienen oxigeno en su molécula. Se forman por la combinación de un no metal con el hidrogeno y su reacción se representa con la ecuación. NO METAL + HIDROGENO HIDRÁCIDO Cloro + Hidrogeno Ácido clorhídrico Cl2 + H2 2HCl Bromo + Hidrogeno Ácido bromhídrico Br2 + H2 2 HBr Azufre + Hidrogeno Ácido sulfhidrico S + H2 H2S SE CLASIFICAN EN : Hidrácidos Oxácidos. Se nombran empleando la palabra genérica ácido seguida del nombre en latín del elemento no metálico con la terminación hídrico.
- 2. OXIÁCIDOS : Son ácidos que contienen oxígeno en su molécula. Se forman al reaccionar un óxido no metálico o anhídrido (combinación de un no metal y el oxígeno), con el agua. ÓXIDO NO METALICO + AGUA OXIÁCIDO Anhídrido carbónico + agua Acido carbónico CO2 + H2O H2CO3 Anhídrido sulfúrico +Agua Ácido sulfúrico SO3 + H2O H2SO3 Anhídrido nítrico + Agua Ácido Nítrico N2O5 + H2O 2HNO3 Los oxácidos se nombran como los anhídridos u óxidos de donde provienen
- 3. TEORIA DE LOS ÁCIDOS Teoría clásica o de Arrhenius. Svante Arrhenius, en 1887, llegó a la conclusión de que las propiedades características de las disoluciones acuosas de los ácidos se debían a los iones hidrógeno, H+, mientras que las propiedades típicas de las bases se debían a iones hidróxido, OH- . CARACTERISTICAS DE LOS ÁCIDOS: Son compuestos que tienen un sabor agrio típico, llamado sabor ácido. Producen una sensación punzante en contacto con la piel. Sus disoluciones acuosas cambian el color de muchos colorantes vegetales; por ejemplo, producen un color rojo con el tornasol (azul). Contiene hidrógeno que puede liberarse, en forma gaseosa, cuando a sus disoluciones acuosas se añade un metal activo, como, por ejemplo, cinc. Disuelven muchas sustancias. Cuando reaccionan con hidróxidos metálicos, pierden todas sus propiedades características. CARACTERISTICAS DE LAS BASES: Tienen sabor amargo característico. Sus disoluciones acuosas producen una sensación suave (jabonosa) al tacto. Sus disoluciones acuosas cambian el color de muchos colorantes vegetales; por ejemplo, devuelven el color azul al tornasol enrojecido por los ácidos. Precipitan muchas sustancias, que son solubles en los ácidos. Pierden todas sus propiedades características cuando reaccionan con un ácido.
- 4. ESCALA DEL P. H. La fuerza de un ácido o una base se determina por medio del P. H. El cual representa la concentracion de iones hidrogeno que posee una solución por medio de una escala de valores
- 5. 3.2 CLASIFICACION DE LAS SALES NEUTRALIZACION Y FORMACION DE SALES Las sales son compuestos que están formados por un metal(catión) más un radical(anión) SE CLASIFICAN EN SALES BINARIAS SALES TERCIARIAS SALES BINARI AS : Las sales binarias son la combinación de no metales con metales y no metales. Se formulan sustituyendo los hidrógenos de los hidruros no metálicos por un metal o un no metal e intercambiando las valencias. KBr bromuro de potasio bromuro de potasio FeCl2 cloruro ferroso cloruro de fierro (II) FeCl3 cloruro férrico cloruro de fierro (III) CuS sulfuro cúprico sulfuro de cobre (II) Una forma simple de determinar la fórmula de la sal es la siguiente EJEMPLO DE NEUTRALIZACION : NaOH + HCl NaCl + H2O Hidróxido más ácido Produce Cloruro más Agua de sodio clorhídrico de sodio HBr + NaOH NaBr + H2O Acido Bromhídrico Hidróxido de Sodio Bromuro de Sodio Agua
- 6. SALES TERCIARIAS : Las sales terciarias se nombran de la siguiente manera. Número de oxígenos con el prefijo correspondiente Nombre del elemento central acabado en -ato Sulfato de Sodio (Na2SO4) es una sustancia incolora, cristalina con buena solubilidad en el agua y mala solubilidad en la mayoría de los disolventes orgánicos con excepción de la glicerina. CaCO3 carbonato de calcio Es una sustancia muy abundante en la naturaleza, formando rocas, como componente principal, en todas partes del mundo, y es el principal componente de conchas y esqueletos de muchos organismos (p.ej. moluscos, corales) o de las cáscaras de huevo
- 7. TIPOS DE REACCIONES QUÍMICAS ¿ QUÉ ES UNA REACCION QUIMICA? TIPOS DE REACCIONES QUÍMICAS Síntesis o combinación directa Descomposición Sustitución simple Sustitución doble Síntesis o combinación directa : Dos o más elementos o compuestos se combinan para formar un solo compuesto 2Hg + O2 2HgO Descomposición : Un compuesto se separa en dos o más elementos o compuestos 2H2O 2H2 + O2 H2SO3 H2O + SO2 H2O + NH3 NH4OH Sustitución simple : Un elemento toma el lugar de otro en un compuesto Zn +CuSO4 ZnSO4 + Cu Fe + 2HCl FeCl2 +H2 Sustitución doble : Dos elementos o radicales de diferentes compuestos se intercambian HCl + NaOH NaCl + H2O AgNO3 + NaCl NaNO3 + AgCl
- 8. BALANCEO DE EQUACIONES POR TANTEO BALANCEAR : Consiste en obtener los coeficientes de cada una de las formulas de las sustancias, (reactivos y productos), y que estos cumplan con la ley de la materia que establece: “ la materia no se crea ni se destruye solo se transforma” “la suma de productos debe ser inversamente proporcional a la suma de productos” Na + Cl NaCl H2 + O2 H2O 1 1 = 2 1 1 = 2 2 2 = 4 2 1 = 3 BALANCEO DE EQUACIONES POR REDOX Se define como la participación de algunos elementos en donde se intercambian valencias Y existe una oxidación y una reducción en el enlace. REACCIÓN DE OXIDACIÓN : Hay sustancias que pueden donar electrones ; son sustancias reducidas que en las condiciones adecuadas se pueden oxidar, y por lo tanto transformarse en formas oxidadas. Veamoslo en el siguiente dibujo : REACCIÓN DE REDUCCIÓN : Hay sustancias que pueden aceptar electrones ; son sustancias oxidadas que en las condiciones adecuadas se pueden reducir, y por lo tanto transformarse en formas reducidas. Veamoslo en el siguiente dibujo :