Rastreo episemologico del enlacequimico
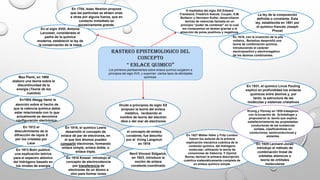
- 1. RASTREO EPISTEMOLOGICO DEL CONCEPTO “ ENLACE QUIMICO” Los primeros planteamientos sobre enlace químico surgieron a principios del siglo XVII, y suponían ciertos tipos de afinidades químicas. En 1704, Isaac Newton propone que las partículas se atraen unas a otras por alguna fuerza, que en contacto inmediato es excesivamente grande. Nevil Vincent Sidgwick, en 1923, introduce la noción de enlace covalente coordinado En1904 Abegg llamó la atención sobre el hecho de que la valencia química debía estar relacionada con lo que actualmente se denomina configuración electrónica. En 1819, con la invención de la pila voltaica, Berzelius desarrolló una teoría de combinación química, introduciendo el carácter electropositivo y electronegativo de los átomos combinantes. A mediados del siglo XIX Edward Frankland, Friedrich Kekulé, Couper, A.M. Butlerov y Hermann Kolbe, desarrollaron teorías de valencias llamada en un principio “poder de combinar” en la cual los compuestos se atraían gracias a la atracción de polos positivos y negativos. En 1913 Bohr publicó una explicación teórica para el espectro atómico del hidrógeno basado en los niveles de energía En 1927 Walter Hitler y Fritz London fueron los autores de la primera explicación mecánica cuántica de la conexión química, del hidrógeno molecular, utilizando la teoría de conexiones de Valencia. Y Oyvind Burrau derivan la primera descripción cuántica matemáticamente completa de un enlace químico simple. el concepto de enlace covalente, fue descrito por el Irving Langmuir en 1919 En 1916 Kossel introdujo el concepto de electrovalencia por transferencia de electrones de un átomo a otro para formar iones En 1916, el químico Lewis desarrolló el concepto de enlace de par de electrones, en el que dos átomos pueden compartir electrones, formando enlace simple, enlace doble, o enlace triple. En 1931, el químico Linus Pauling explicó en profundidad los enlaces químicos entre átomos y, por tanto, la estructura de las moléculas y sistemas cristalinos En 1912 el descubrimiento de la difracción de rayos X por los cristales por Laue En el siglo XVIII, Antoine Lavoisier, considerado el padre de la química moderna, estableció la ley de la conservación de la masa En 1929 Lennard-Jones introdujo el método de combinación lineal de orbitales atómicos o teoría de orbitales moleculares Drude a principios de siglo XX propuso la teoría del enlace metálico, recibiendo el nombre de teoría del electrón libre o del mar de electrones Max Plank, en 1900 elaboro una teoría sobre la discontinuidad de la energía (Teoría de los cuantos) La ley de la composición definida o constante. Esta ley, establecida en 1801 por el químico francés Joseph Proust Kronig y Penney en 1930 trabajaron con la ecuación de Schrödinger y propusieron la teoría que explica satisfactoriamente las propiedades conductoras de las sustancias solidas, clasificándolas en conductoras, semiconductoras y aislantes