Isosteros y bioisosterismo
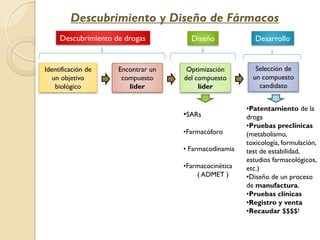
- 1. Descubrimiento y Diseño de Fármacos Identificación de un objetivo biológico Encontrar un compuesto líder Optimización del compuesto líder Selección de un compuesto candidato •SARs •Farmacóforo • Farmacodinamia •Farmacocinética ( ADMET ) Descubrimiento de drogas Diseño Desarrollo •Patentamiento de la droga •Pruebas preclínicas (metabolismo, toxicología, formulación, test de estabilidad, estudios farmacológicos, etc.) •Diseño de un proceso de manufactura. •Pruebas clínicas •Registro y venta •Recaudar $$$$!
- 2. Variación de los sustituyentes Extensión de la estructura Extensión o contracción de cadenas o anillos Variaciones de anillos Fusiones de anillos Reemplazos Isóstericos y bioisóstericos Simplificación de la estructura Rigidización de la estructura Optimización del compuesto líder • Identificar las relaciones de estructura-actividad (SARs). • Identificar el farmacóforo (atomos o grupos funcionales requeridos para una específica actividad farmacológica, y sus posiciones relativas en el espacio). • Mejorar la interacción con su objetivo biológico (Farmacodinamia) – Unión al receptor, efectos en el organismo, ventana terapéutica, efectos indeseables. • Mejorar las propiedades farmacocinéticas – ADME T Reemplazos Isóstericos y bioisostéricos
- 3. Variaciones moleculares basadas en reemplazos iso-bioistéricos ISÓSTEROS: átomos o grupos de átomos que presentan características electrónicas y estéricas similares BIOISÓSTEROS: (isósteros no clásicos) átomos o grupos de átomos que presentan propiedades biológicas similares (aunque la semejanza fisicoquímica sea vaga) Isósteros bivalentes
- 4. Reemplazos Isostéricos: • Mejorar la interacción con su objetivo biológico (Farmacodinamia) – Unión al receptor, efectos en el organismo, ventana terapéutica, efectos indeseables. • Mejorar las propiedades farmacocinéticas – Absorción Distribución Metabolismo Excreción Optimización de propiedades : Hidro/lipofílicas (LogP) interacción con receptores, paso a través de las membranas Polaridad Pka Modificaciones que afecten la metabolización
- 5. Reemplazos isostéricos Clasificación: Átomos o grupos univalentes Átomos o grupos divalentes Átomos o grupos trivalentes Anillos equivalentes Grupos con efectos polares similares: Biosisot. de ácidos carboxílicos Biosisot. de ésteres carboxílicos Bioisost. del enlace carboxamida Biosisot. de urea Biosisot. de fenol Biosisot. de catecol Biosisot. de sulfonamida Inversión de grupos funcionales
- 6. Reemplazos isostéricos Clasificación: Átomos o grupos univalentes Anti tumor agentsMetabolic product
- 7. Reemplazos isostéricos Clasificación: Átomos o grupos divalentes
- 8. Reemplazos isostéricos Clasificación: Átomos o grupos divalentes
- 9. Reemplazos isostéricos Clasificación: Átomos o grupos divalentes
- 10. Reemplazos isostéricos: Átomos o grupos univalentes Átomos o grupos divalentes Átomos o grupos trivalentes Grupos con efectos polares similares: Biosisot. de ácidos carboxílicos Biosisot. de ésteres carboxílicos Bioisost. del enlace carboxamida Biosisot. de urea, Biosisot. de fenol Biosisot. de catecol Biosisot. de sulfonamida Inversión de grupos funcionales Anillos equivalentes
- 13. Reemplazos isostéricos: Átomos o grupos univalentes Átomos o grupos divalentes Átomos o grupos trivalentes Anillos equivalentes Grupos con efectos polares similares: Biosisot. de ácidos carboxílicos Biosisot. de ésteres carboxílicos Bioisost. del enlace carboxamida Biosisot. de urea, Biosisot. de fenol Biosisot. de catecol Biosisot. de sulfonamida Inversión de grupos funcionales
- 14. Biosisot. de ésteres carboxílicos Molécula con una mayor estabilidad metabólica, (t1/2= 61 h)
- 15. Reemplazos isostéricos: Átomos o grupos univalentes Átomos o grupos divalentes Átomos o grupos trivalentes Anillos equivalentes Grupos con efectos polares similares: Biosisot. de ácidos carboxílicos Biosisot. de ésteres carboxílicos Bioisost. del enlace carboxamida Biosisot. de urea, Biosisot. de fenol Biosisot. de catecol Biosisot. de sulfonamida Inversión de grupos funcionales
- 16. Bioisost. del enlace carboxamida : clásicos
- 17. Bioisost. del enlace carboxamida: no clásicos Los que más se aproximan en el reemplazo del enlace peptídico
- 18. Biosisósteros de urea tiourea cianoguanidina diaminonitroetileno
- 19. Inversión de grupos funcionales Generalmente usado en química de péptidos Similares valores de inhibición de endopeptidasa neutral y de termolisina . Diferencias en la inhibicion de la Enz. Convertidora de angiotensina.
- 20. Inversión de grupos funcionales No peptídicos
- 22. Conversión química o transformación, de fármacos o sustancias endógenas en compuestos más fáciles de eliminar. Metabolismo: metabolitos activos metabolitos inactivos productos metabólicos con menor, mayor o distinta actividad farmacológica.
- 26. Hidrólisis: Amidas se hidrolizan más lento que los ésteres
- 27. Modificaciones que hacen a las drogas más resistentes al metabolismo Grupo Protector estérico: Bioisósteros de grupos polares: Bloqueadores de metabolismo: Remoción, reemplazo de grupos metabólicamente susceptibles:
- 28. Remoción o reemplazo de grupos metabólicamente lábiles: Variación de anillos o sustituyentes de anillos: Imidazol es más susceptible a metabolización que el triazol.
- 29. Modificaciones que hacen a las drogas menos resistentes al metabolismo Introducción de grupos metabólicamente lábiles:
- 30. Prodrogas Compuestos inactivos por sí mismos, pero que son convertidos a moléculas activas en el organismo, generalmente mediante una reacción enzimática. Ésteres:
- 31. Análisis de las Modificaciones Isostéricas: compuesto líder compuesto modificado Actividad Potencia Selectividad ADME Toxicidad Efectos indeseables Aumento, disminución o anulación de: