22 diagrama de fases
•
0 recomendaciones•510 vistas
química general primaria secundaria academia Profesor Adolfo Ramón pueden descargarlo en: http://radolperu.wix.com/quimica_general
Denunciar
Compartir
Denunciar
Compartir
Más contenido relacionado
La actualidad más candente
La actualidad más candente (20)
Dilatación de sólidos y líquidos y Comportamiento anómalo del agua.

Dilatación de sólidos y líquidos y Comportamiento anómalo del agua.
Uso de tablas termodinámicas. Equilibrio líquido-vapor

Uso de tablas termodinámicas. Equilibrio líquido-vapor
Similar a 22 diagrama de fases
Similar a 22 diagrama de fases (20)
Más de Adolfo Luis Ramon
Más de Adolfo Luis Ramon (20)
Último
Último (20)
Caja de herramientas de inteligencia artificial para la academia y la investi...

Caja de herramientas de inteligencia artificial para la academia y la investi...
plande accion dl aula de innovación pedagogica 2024.pdf

plande accion dl aula de innovación pedagogica 2024.pdf
ACUERDO MINISTERIAL 078-ORGANISMOS ESCOLARES..pptx

ACUERDO MINISTERIAL 078-ORGANISMOS ESCOLARES..pptx
BIOMETANO SÍ, PERO NO ASÍ. LA NUEVA BURBUJA ENERGÉTICA

BIOMETANO SÍ, PERO NO ASÍ. LA NUEVA BURBUJA ENERGÉTICA
MAYO 1 PROYECTO día de la madre el amor más grande

MAYO 1 PROYECTO día de la madre el amor más grande
Curso = Metodos Tecnicas y Modelos de Enseñanza.pdf

Curso = Metodos Tecnicas y Modelos de Enseñanza.pdf
Plan Refuerzo Escolar 2024 para estudiantes con necesidades de Aprendizaje en...

Plan Refuerzo Escolar 2024 para estudiantes con necesidades de Aprendizaje en...
ACERTIJO DE POSICIÓN DE CORREDORES EN LA OLIMPIADA. Por JAVIER SOLIS NOYOLA

ACERTIJO DE POSICIÓN DE CORREDORES EN LA OLIMPIADA. Por JAVIER SOLIS NOYOLA
Lecciones 05 Esc. Sabática. Fe contra todo pronóstico.

Lecciones 05 Esc. Sabática. Fe contra todo pronóstico.
22 diagrama de fases
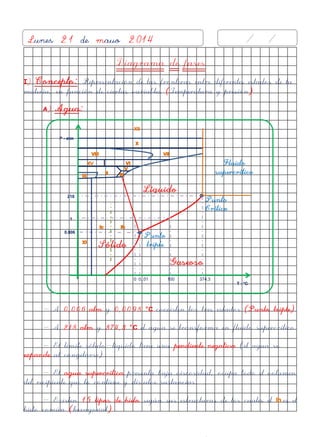
- 1. Diagrama de fases I) Concepto: Representación de las fronteras entre diferentes estados de la materia, en función de ciertas variables (Temperatura y presión) A) Agua: 0 0,.01 100 374,3 - A 0,006 atm y 0,0098 °C coexisten los tres estados (Punto triple) - A 218 atm y 374,3 °C el agua se transforma en fluido supercrítico. - El límite sólido-líquido tiene una pendiente negativa (el agua se expande al congelarse) - El agua supercrítica presenta baja viscosidad, ocupa todo el volumen del recipiente que lo contiene y disuelve sustancias. - Existen 15 tipos de hielo según sus estructuras de los cuales el es el hielo común (hexagonal) Punto triple Lunes 21 de mayo 2014 / / Sólido Líquido Gaseoso Fluido supercrítico 0,006 1 218 P - atm T - °C Punto Crítico
- 2. B) Dióxido de carbono:CO2 - A 5,2 atm y - 56,4 °C coexisten los tres estados (Punto triple) - A 218 atm y 374 °C el CO2 se transforma en fluido supercrítico. - El límite sólido-líquido tiene una pendiente positiva (el CO2 se contrae al congelarse) - El CO2 supercrítica presenta baja viscosidad, ocupa todo el volumen del recipiente que lo contiene y disuelve sustancias. - La ventaja sobre el agua supercrítica es que el CO2 supercrítico se obtiene a temperaturas relativamente bajas (31,1 °C) Compuesto Temperatura crítica/K Presión crítica/MPa 1. Xenón 2. Etano 3. Amoniaco 289,8 305,4 405,6 5,12 4,88 11,28 Fluido supercrítico Punto triple P - atm T - °C Punto Crítico Sólido Líquido Gaseoso 73 5,2 1 - 78 - 56,4 31,1 / /
