8 sistemas químicos
•
0 recomendaciones•4,018 vistas
química general primaria secundaria academia Profesor Adolfo Ramón pueden descargarlo en: http://radolperu.wix.com/quimica_general
Denunciar
Compartir
Denunciar
Compartir
Más contenido relacionado
La actualidad más candente
La actualidad más candente (20)
Clase 3 biomoléculas inorgánicas agua y sales minerales

Clase 3 biomoléculas inorgánicas agua y sales minerales
Niveles de Organizacion de los Seres Vivos (Actividad para Examen Final)

Niveles de Organizacion de los Seres Vivos (Actividad para Examen Final)
Propiedades generales y particulares de la materia

Propiedades generales y particulares de la materia
Destacado (15)
Similar a 8 sistemas químicos
Similar a 8 sistemas químicos (20)
Formacion para el proyecto de quimiica para presentar

Formacion para el proyecto de quimiica para presentar
Unidad N°1 Biología-El Agua-Teoría de sistemas-.pdf

Unidad N°1 Biología-El Agua-Teoría de sistemas-.pdf
Más de Adolfo Luis Ramon
Más de Adolfo Luis Ramon (20)
Último
Último (20)
Sesión de aprendizaje Planifica Textos argumentativo.docx

Sesión de aprendizaje Planifica Textos argumentativo.docx
Planificacion Anual 2do Grado Educacion Primaria 2024 Ccesa007.pdf

Planificacion Anual 2do Grado Educacion Primaria 2024 Ccesa007.pdf
Curso = Metodos Tecnicas y Modelos de Enseñanza.pdf

Curso = Metodos Tecnicas y Modelos de Enseñanza.pdf
Estrategia de prompts, primeras ideas para su construcción

Estrategia de prompts, primeras ideas para su construcción
Tema 8.- PROTECCION DE LOS SISTEMAS DE INFORMACIÓN.pdf

Tema 8.- PROTECCION DE LOS SISTEMAS DE INFORMACIÓN.pdf
La empresa sostenible: Principales Características, Barreras para su Avance y...

La empresa sostenible: Principales Características, Barreras para su Avance y...
RETO MES DE ABRIL .............................docx

RETO MES DE ABRIL .............................docx
TIPOLOGÍA TEXTUAL- EXPOSICIÓN Y ARGUMENTACIÓN.pptx

TIPOLOGÍA TEXTUAL- EXPOSICIÓN Y ARGUMENTACIÓN.pptx
el CTE 6 DOCENTES 2 2023-2024abcdefghijoklmnñopqrstuvwxyz

el CTE 6 DOCENTES 2 2023-2024abcdefghijoklmnñopqrstuvwxyz
Clasificaciones, modalidades y tendencias de investigación educativa.

Clasificaciones, modalidades y tendencias de investigación educativa.
Planificacion Anual 4to Grado Educacion Primaria 2024 Ccesa007.pdf

Planificacion Anual 4to Grado Educacion Primaria 2024 Ccesa007.pdf
8 sistemas químicos
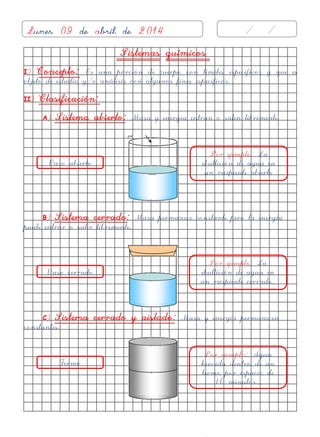
- 1. Sistemas químicos I) Concepto: Es una porción de cuerpo con límites específicos y que es objeto de estudio y/o análisis con algunos fines específicos. II) Clasificación: A) Sistema abierto: Masa y energía entran o salen libremente. B) Sistema cerrado: Masa permanece constante pero la energía puede entrar o salir libremente. C) Sistema cerrado y aislado: Masa y energía permanecen constantes. Vaso abierto Vaso cerrado Termo Por ejemplo: La ebullición de agua en un recipiente abierto Por ejemplo: La ebullición de agua en un recipiente cerrado. Por ejemplo: Agua hervida dentro de un termo por espacio de 10 minutos.. Lunes 09 de abril de 2014 / /
- 2. II) Partes: 1. Medio Externo: Es todo aquello que rodea el sistema. 2. Pared del Sistema: Es el medio material que separa el medio externo y el sistema propiamente dicho. 3. Fase: Es toda materia (masa) homogénea, por lo tanto las sustancias puras y mezclas homogéneas, cada una constituyen una sola fase. 4. Interface: Es el medio que separa dos fases. 5. Componente: Es el tipo de sustancia química (simple o compuesta) presente en el sistema. Ejemplos: 1) Mezcla de agua y hielo > Tiene dos fases: H2O (l) H2O (s), sistema difásico > Tiene solo un componente: H2O, Sistema unitario . 2) Mezcla de agua, hielo seco y vapor > Tres fases: Agua, H2O y vapor, sistema trifásico > Tiene Dos componentes: H2O y CO2, Sistema binario
