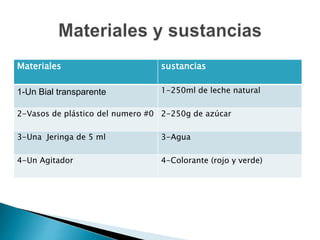
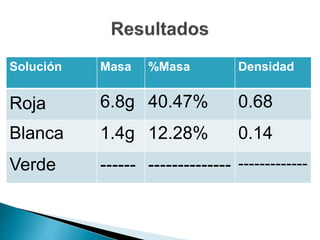
El documento describe un experimento para crear una 'bandera' con tres soluciones de diferentes densidades utilizando colorantes. Se explica cómo las diferencias en densidad entre las soluciones roja, blanca y verde permiten que se mantengan separadas en un recipiente, cumpliendo con el objetivo del experimento. Además, se definen términos clave como mezcla homogénea, mezcla heterogénea y diferentes tipos de soluciones.