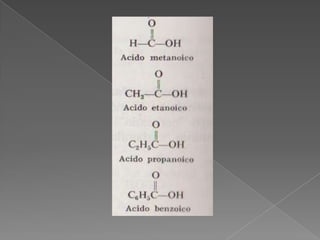
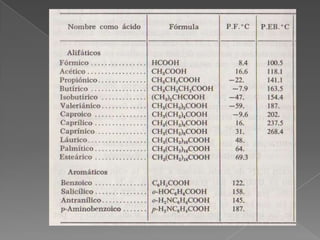
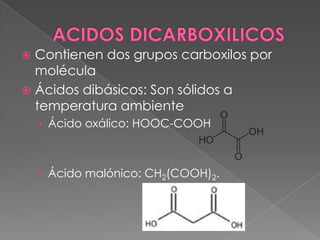
Los ácidos orgánicos se caracterizan por contener un grupo carboxilo. Pueden formar dímeros mediante puentes de hidrógeno y sales al reaccionar con metales u otras bases. Muchos ácidos carboxílicos tienen olores fuertes debido a su bajo peso molecular y volatilidad.