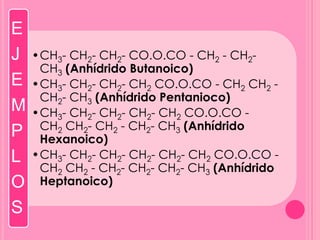
Los anhídridos de ácido son compuestos orgánicos cuya fórmula general es (RCO)2O que se forman por la condensación de dos moléculas de ácido carboxílico con pérdida de una molécula de agua. Pueden ser simples (los ácidos son iguales) o mixtos (los ácidos son diferentes). Se obtienen calentando ácidos carboxílicos o reaccionando haluros de alcanoilo con ácidos. El anhídrido acético es un compuesto importante