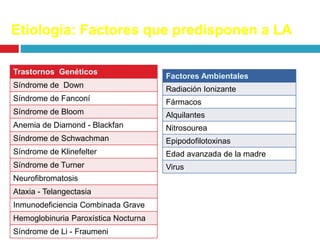
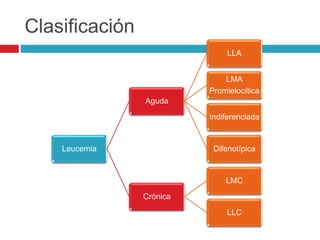
La leucemia aguda en pediatría es la neoplasia maligna más frecuente en niños, representando alrededor del 30-40% de los cánceres infantiles. La leucemia linfoblástica aguda (LLA) es el tipo más común, representando aproximadamente el 75-80% de los casos. Los síntomas iniciales suelen ser inespecíficos como fiebre, dolor óseo y articulaciones, cefalea, linfadenopatías y manifestaciones de insuficiencia medular como anemia y trombocitopenia