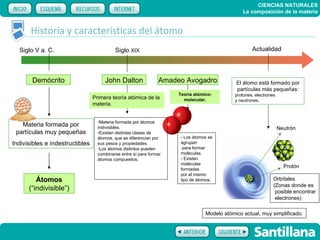
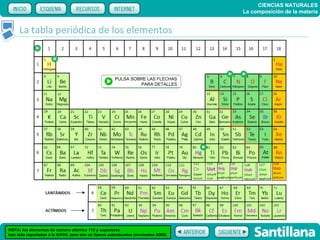
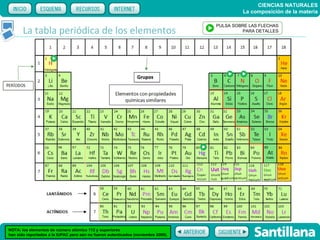
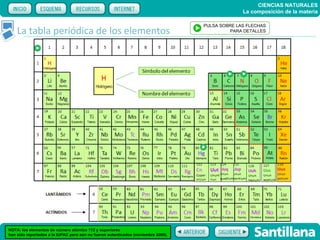
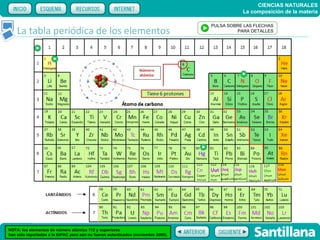
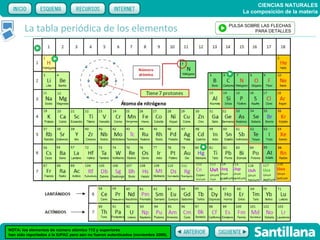
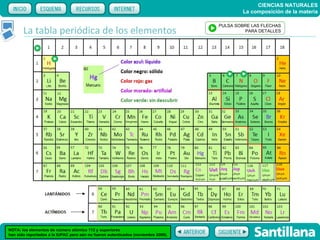
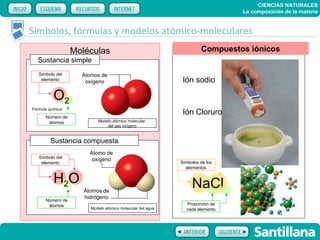
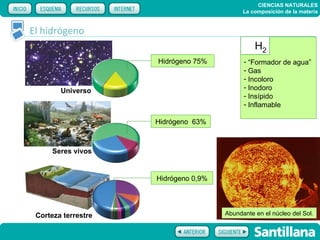
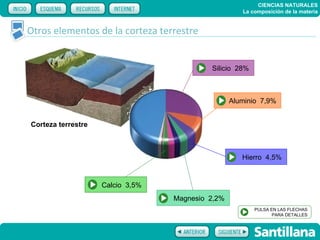
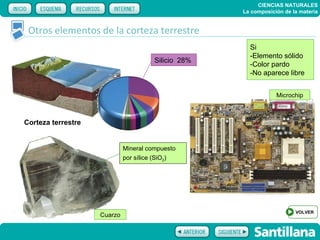
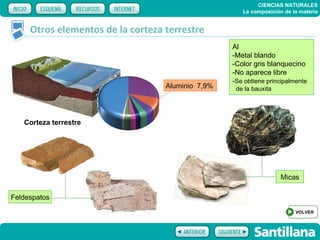
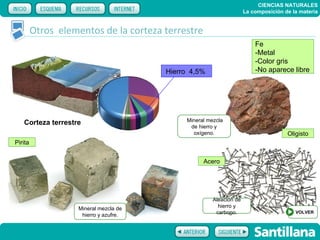
El documento trata sobre la composición de la materia. Explica la historia del átomo y su estructura actual, incluyendo protones, electrones y neutrones. También describe la tabla periódica de los elementos, los diferentes estados de la materia, y elementos clave como el hidrógeno, oxígeno y carbono. Proporciona recursos para explicar estas ideas fundamentales sobre la composición química de la materia.