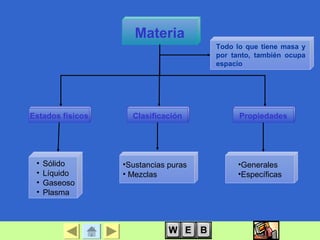
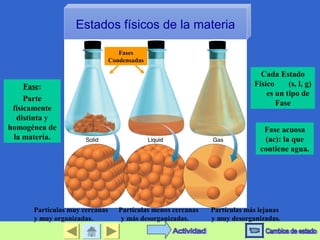
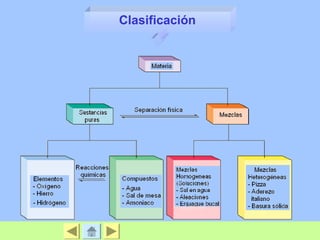
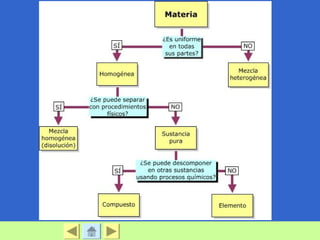
Este documento trata sobre la materia y sus propiedades. Explica que la materia puede existir en diferentes estados físicos como sólido, líquido y gas. También describe las propiedades físicas y químicas que permiten caracterizar y distinguir entre sustancias. Finalmente, explica diferentes métodos para separar mezclas como filtración, destilación y evaporación.