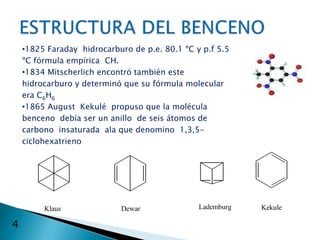
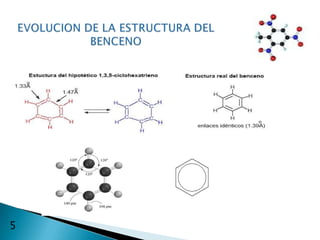
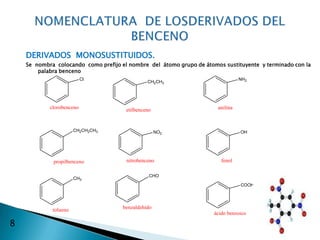
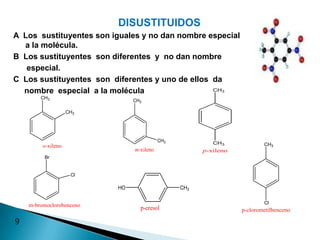
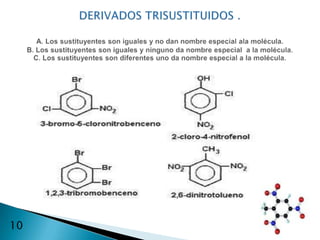
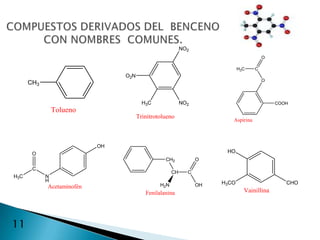
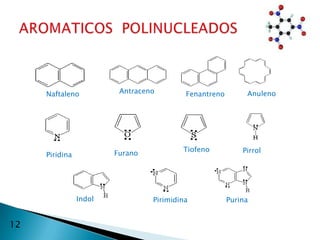
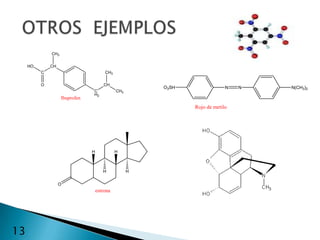
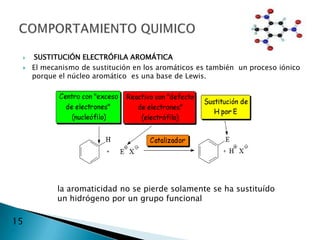
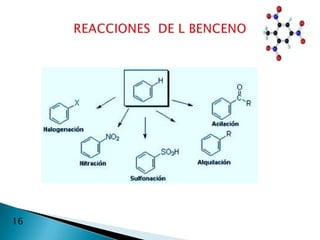
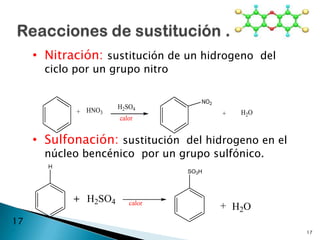
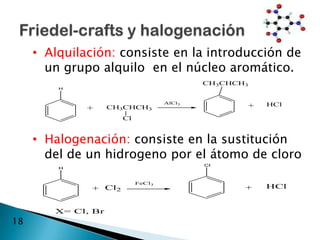
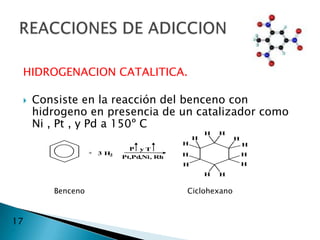
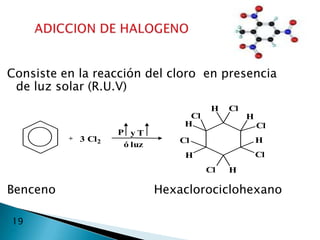
El documento describe la química de los compuestos aromáticos como el benceno y sus derivados. Explica la estructura resonante del benceno y cómo se forman sus derivados mediante sustitución electrófila aromática. También cubre reacciones como la nitración, sulfonación, alquilación y halogenación de compuestos aromáticos.