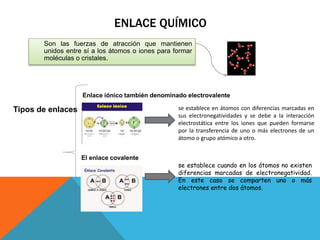
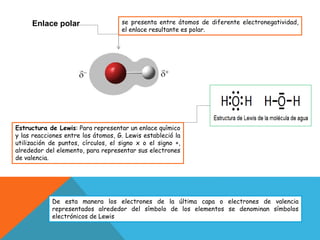
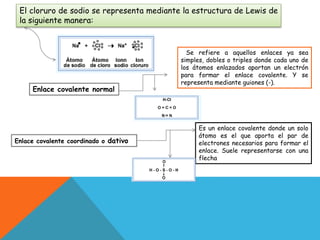
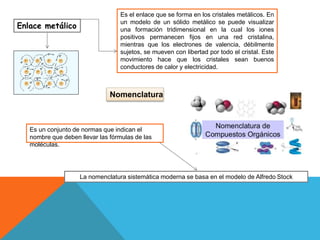
El documento habla sobre los diferentes tipos de enlaces químicos, incluyendo enlaces iónicos, covalentes y metálicos. Explica que los enlaces iónicos involucran la transferencia de electrones entre átomos, mientras que los enlaces covalentes comparten electrones. También describe la estructura de Lewis para representar enlaces químicos y la nomenclatura de compuestos inorgánicos como óxidos, ácidos y sales.