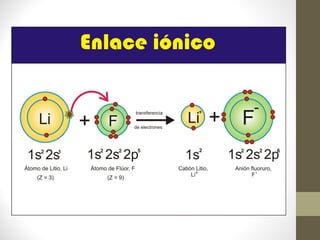
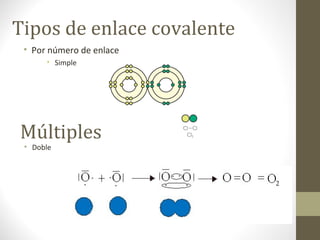
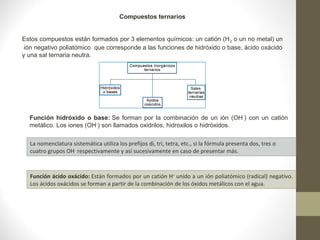
El documento describe los diferentes tipos de enlaces químicos, incluyendo enlace iónico, covalente y metálico. Explica las propiedades de los compuestos formados por cada tipo de enlace y cómo se determina el tipo de enlace basado en la electronegatividad de los átomos involucrados. También resume los diferentes tipos de nomenclatura química y tipos de compuestos como binarios y ternarios.