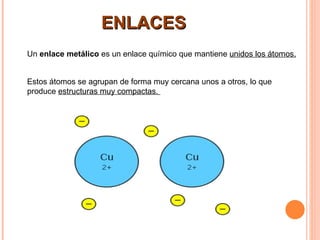
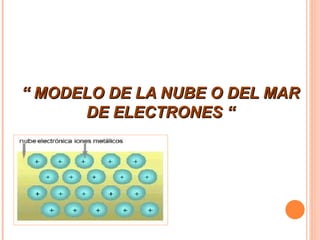
Este documento describe el enlace metálico. Los átomos en un metal se agrupan muy juntos en una red tridimensional compacta y comparten electrones, formando una "nube de electrones" que mantiene unida la estructura. Los metales tienden a ser sólidos, brillantes, maleables y buenos conductores de calor y electricidad. El modelo atómico explica que los átomos metálicos pierden electrones para formar iones positivos ordenados en una red, mientras que los electrones comparten se mueven libremente por toda la e