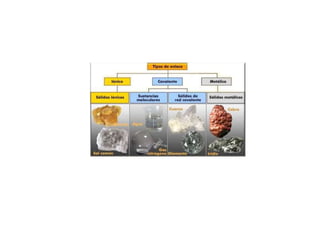
Los átomos se unen a través de tres tipos principales de enlaces: iónicos, covalentes y metálicos. Los enlaces iónicos involucran la transferencia de electrones entre átomos metálicos y no metálicos, formando iones con cargas opuestas atraídas entre sí. Los enlaces covalentes ocurren cuando átomos no metálicos comparten pares de electrones. Los enlaces metálicos involucran la pérdida de electrones por átomos metálicos que forman una nube de electrones que