ENLACE METALICO.pptx
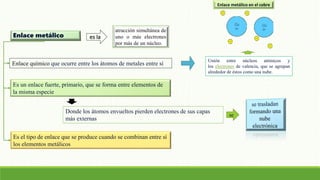
- 1. es la atracción simultánea de uno o más electrones por más de un núcleo. Enlace químico que ocurre entre los átomos de metales entre sí Unión entre núcleos atómicos y los electrones de valencia, que se agrupan alrededor de éstos como una nube. Es un enlace fuerte, primario, que se forma entre elementos de la misma especie Es el tipo de enlace que se produce cuando se combinan entre sí los elementos metálicos Donde los átomos envueltos pierden electrones de sus capas más externas se Enlace metálico en el cobre
- 2. Los átomos de los metales se agrupan de forma muy cercana unos a otros, lo que produce estructuras muy compactas. En este tipo de estructura cada átomo metálico está rodeado por otros doce átomos (seis en el mismo plano, tres por encima y tres por debajo). Debido a la baja electronegatividad que poseen los metales, los electrones de valencia son extraídos de sus orbitales y tienen la capacidad de moverse libremente a través del compuesto metálico, lo que otorga a éste las propiedades eléctricas y térmicas. Los elementos con un enlace metálico están compartiendo un gran número de electrones de valencia, formando un mar de electrones rodeando un enrejado gigante de cationes. Muchos de los metales tienen puntos de fusión más altos que otros elementos no metálicos, por lo que se puede inferir que hay enlaces más fuertes entre los distintos átomos que los componen. La vinculación metálica es no polar, apenas hay diferencia de electronegatividad entre los átomos que participan en la interacción de la vinculación (en los metales elementales puros) o muy poca (en las aleaciones), y los electrones implicados en lo que constituye la interacción a través de la estructura cristalina del metal.
- 3. Supóngamos el metal cobre En el cobre sus átomos Cu ceden sus electrones de valencia para formar el enlace metálico. Arriba este enlace se representa como cationes Cu2+ (círculos azules) rodeados de electrones (círculos amarillos). Los electrones no están quietos: se mueven por todo el cristal de cobre. No obstante, en los metales no se habla formalmente de cationes, sino de átomos metálicos neutros.
- 4. El enlace metálico explica muchas características físicas de las sustancias metálicas, tales como fuerza, maleabilidad, ductilidad, conducción de calor y de la electricidad, y brillo o lustre (devuelven la mayor parte de la energía lumínica que reciben). La vinculación metálica es la atracción electrostática entre los átomos del metal o cationes y los electrones deslocalizados. Los átomos del metal tienen por lo menos un electrón de valencia No comparten electrones con los átomos vecinos No pierden electrones para formar los iones En lugar los niveles de energía externos de los átomos del metal se traslapan
- 5. En las estructuras metálicas no se habla propiamente de moléculas, sino de átomos neutros (o cationes, según otras perspectivas El enlace metálico tiene la propiedad de reorganizarse. Esto no ocurre con los enlaces covalente e iónico. Si un enlace covalente se parte, no volverá a formarse como si no hubiera ocurrido nada La propiedad que tiene el enlace metálico de tener sus electrones deslocalizados le confiere además a los metales la capacidad de conducir el calor y la electricidad Los electrones deslocalizados y móviles también pueden interaccionar con los fotones de la luz visible y rechazarlos. Los casos más excepcionales son los del cobre, mercurio y oro, que absorben fotones de ciertas frecuencias.
- 6. Ejemplos de enlaces metálicos Zinc Oro (Au) Cobre (Cu) Plata (Ag) Níquel (Ni) Cadmio (Cd) Platino (Pt) Titanio (Ti) Plomo (Pb) Acero común Acero inoxidable Bronce Aleaciones de mercurio Aleación de cromo y platino Pieltre Latón
- 7. Existen dos modelos que explican la formación del enlace metálico. MODELO DE LA NUBE DE ELECTRONES TEORÍA DE BANDAS
- 8. Modelo de la nube de electrones Según este modelo, los átomos metálicos ceden sus electrones de valencia a una nube electrónica que comprende todos los átomos del metal. En el enlace metálico, los electrones no pertenecen a ningún átomo determinado. Además, es un enlace no dirigido, porque la nube electrónica es común a todos los restos atómicos que forman la red. Los átomos cuando han cedido los electrones a la nube común, no son realmente iones, ya que los electrones quedan dentro de la red, perteneciendo a todos los restos positivos. Este modelo sirve para interpretar las propiedades de los metales; aunque tiene ciertas limitaciones, principalmente en la explicación de la diferente conductividad de algunos metales. Así pues, el enlace metálico resulta de las atracciones electrostáticas entre los restos positivos y los electrones móviles que pertenecen en su conjunto a la red metálica.
- 9. Esta teoría mantiene que cuando dos átomos enlazan, los orbitales de la capa de valencia se combinan para formar dos orbitales nuevos que pertenecen a toda la molécula, uno que se denomina enlazante (de menor energía) y otro antienlazante (de mayor energía). Si se combinasen 3 átomos se formarían 3 orbitales moleculares, con una diferencia de energía entre ellos menor que en el caso anterior. En general, cuando se combinan N orbitales, de otros tantos átomos, se obtienen N orbitales moleculares de energía muy próxima entre sí, constituyendo lo que se llama una banda. En los metales existe un número muy grande de orbitales atómicos para formar enlaces deslocalizados que pertenezcan a toda la red metálica (como si fuese una gran molécula). Como el número de orbitales moleculares es muy grande forman una banda en la que los niveles de energía, como se ha dicho anteriormente, están muy próximos.
- 10. • Whitten, Davis, Peck & Stanley. (2008). Química. (8va ed.). CENGAGE Learning. • Shiver & Atkins. (2008). Química Inorgánica. (Cuarta edición). Mc Graw Hill. • Wikipedia. (2020). Metallic bonding. Recuperado de: en.wikipedia.org • The Editors of Encyclopaedia Britannica. (2016). Metallic bond. Encyclopædia Britannica. Recuperado de: britannica.com • Helmenstine, Anne Marie, Ph.D. (2020). Metallic Bond: Definition, Properties, and Examples. Recuperado de: thoughtco.com • Jim Clark. (2019). Metallic Bonding. Chemistry LibreTexts. Recuperado de: chem.libretexts.org • Mary Ellen Ellis. (2020). What is a Metallic Bond? Definition, Properties & Examples. Study. Recuperado de: study.com