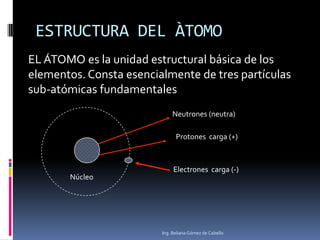
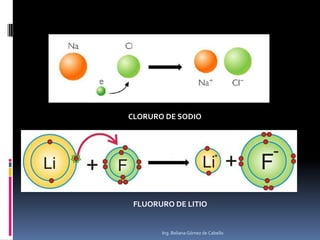
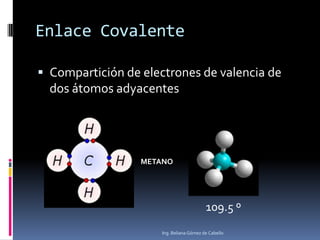
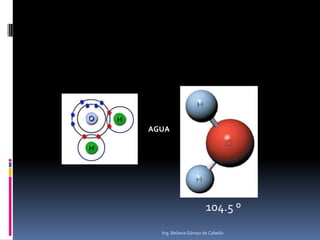
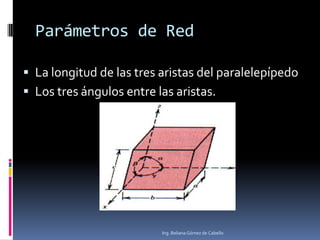
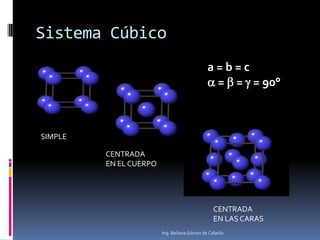
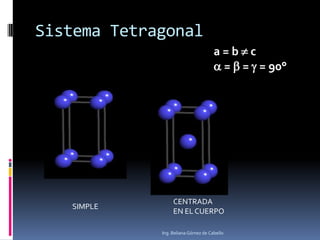
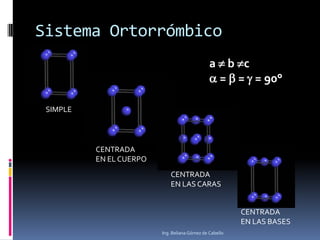
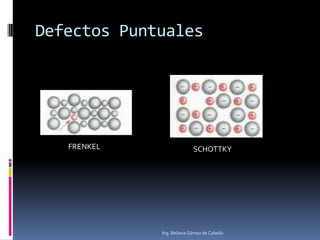
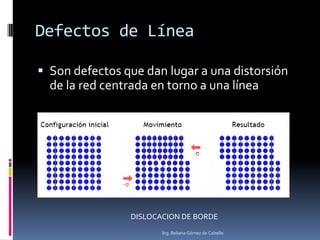
El documento describe la estructura atómica y los tipos de enlaces entre átomos. Explica que el átomo está compuesto de protones, neutrones y electrones, y que los modelos atómicos han evolucionado de un modelo planetario a uno cuántico. También describe los diferentes tipos de enlaces como iónico, covalente y metálico, así como los defectos en la estructura cristalina de los materiales.