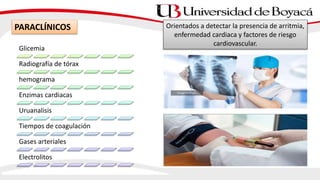
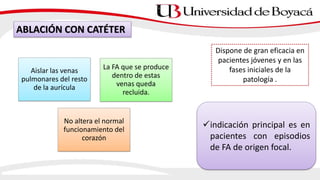
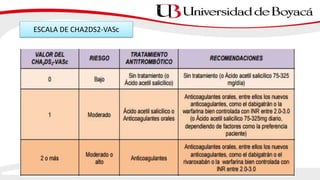
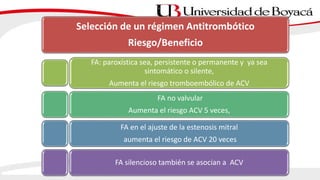
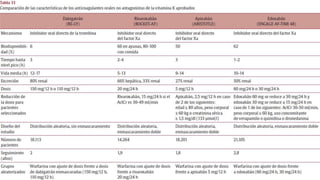
1) El documento presenta información sobre la fibrilación auricular, incluyendo su definición, clasificación, factores de riesgo, mecanismos, tratamiento y escalas de riesgo de accidente cerebrovascular.
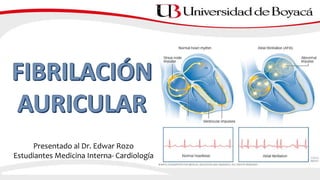
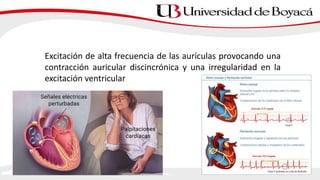
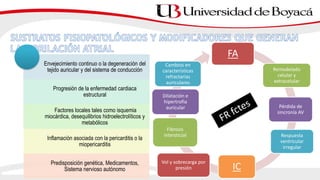
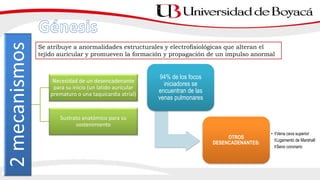
2) La fibrilación auricular se caracteriza por una activación auricular desordenada y es la arritmia sostenida más frecuente. Puede clasificarse según su presentación, duración y etiología.
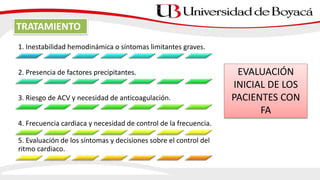
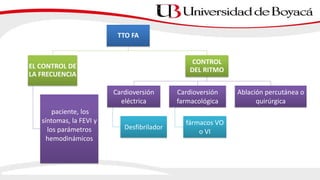
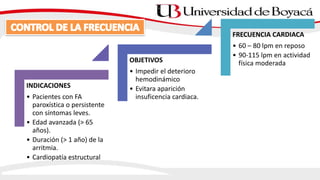
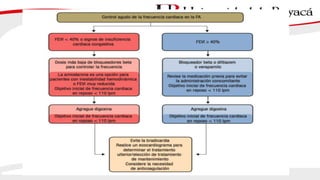
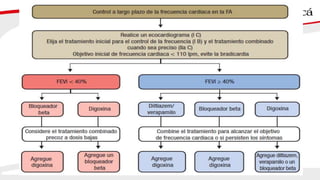
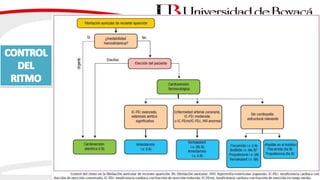
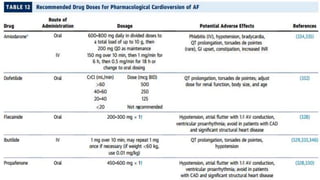
3) El tratamiento incluye el control de la frecuencia cardíaca, cardioversión eléctrica o farmacol