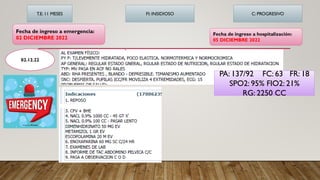
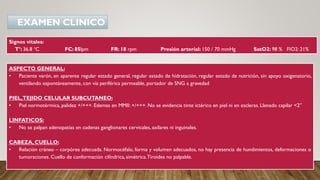
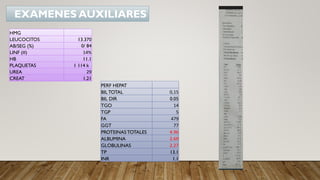
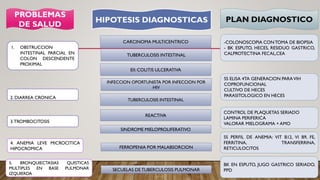
Este documento presenta el caso clínico de un paciente masculino de 35 años con una obstrucción intestinal parcial y diarrea crónica. Se detallan sus antecedentes médicos, exámenes físicos y de laboratorio realizados. El resumen diagnóstico incluye tuberculosis intestinal, colitis ulcerativa, infección oportunista y carcinoma intestinal. Se propone un plan de pruebas que incluye colonoscopia, exámenes de esputo y heces, y estudios para descartar VIH e infecciones.