Guía 1 - Química 10 Funciones Inorgánicas
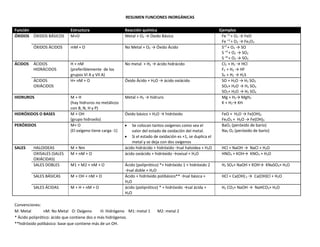
- 1. RESUMEN FUNCIONES INORGÁNICAS Función Estructura Reacción química Ejemplos ÓXIDOS ÓXIDOS BÁSICOS M+O Metal + O2 → Óxido Básico Fe +2 + O2 → FeO Fe +3 + O2 → Fe2O3 ÓXIDOS ÁCIDOS mM + O No Metal + O2 → Óxido Ácido S+2 + O2 → SO S +4 + O2 → SO2 S +6 + O2 → SO3 ÁCIDOS ÁCIDOS HIDRÁCIDOS H + nM (preferiblemente de los grupos VI A y VII A) No metal + H2 → ácido hidrácido Cl2 + H2 → HCl F2 + H2 → HF S4 + H2 → H2S ÁCIDOS OXIÁCIDOS H+ nM + O Óxido Ácido + H2O → ácido oxiácido SO + H2O → H2 SO2 SO2+ H2O → H2 SO3 SO2+ H2O → H2 SO4 HIDRUROS M + H (hay hidruros no metálicos con B, N, H y P) Metal + H2 → hidruro Mg + H2→ MgH2 K + H2→ KH HIDRÓXIDOS O BASES M + OH (grupo hidroxilo) Óxido básico + H2O → hidróxido FeO + H2O → Fe(OH)2 Fe2O3 + H2O → Fe(OH)3 PERÓXIDOS M+ O (El oxígeno tiene carga -1) Se colocan tantos oxígenos como sea el valor del estado de oxidación del metal. Si el estado de oxidación es +1, se duplica el metal y se deja con dos oxígenos BaO2 (peróxido de bario) Na2 O2 (peróxido de bario) SALES HALOIDEAS M + Nm ácido hidrácido + hidróxido →sal haloidea + H2O HCl + NaOH → NaCl + H2O OXISALES (SALES OXIÁCIDAS) M + nM + O ácido oxiácido + hidróxido →oxisal + H2O HNO3 + KOH→ KNO3 + H2O SALES DOBLES M1 + M2 + nM + O Ácido (poliprótico) *+ hidróxido 1 + hidróxido 2 →sal doble + H2O H2 SO4+ NaOH + KOH→ KNaSO4+ H2O SALES BÁSICAS M + OH + nM + O Ácido + hidróxido polibásico** →sal básica + H2O HCl + Ca(OH)2 → Ca(OH)Cl + H2O SALES ÁCIDAS M + H + nM + O ácido (poliprótico) * + hidróxido →sal ácida + H2O H2 CO3+ NaOH → NaHCO3+ H2O Convenciones: M: Metal nM: No Metal O: Oxígeno H: Hidrógeno M1: metal 1 M2: metal 2 * Ácido poliprótico: ácido que contiene dos o más hidrógenos. **hidróxido polibásico: base que contiene más de un OH.
- 2. TALLER NOMENCLATURA QUÍMICA GRADO 10° PARTE I 1. Clasificar los siguientes compuestos según su función química: a) NaNO3 b) AlCl3 c) H2S d) NaH e) MgO f) Mg (OH)2 g) Mn2O3 h) CuSO3 i) HCl j) P2O5 k) Fe2O3 l) AgOH m) Ni(OH)3 n) NaCl o) NO3 p) MgCl2 q) SiO2 r) HBrO2 s) HIO4 t) H3PO3 u) HI v) NiH3 w) HNO3 x) SO2 y) CaCO3 z) Fe(OH)2 Hidruros Óxidos Ácidos Hidróxidos (Bases) Sales Ácidos Básicos Hidrácidos Oxiácidos Haloideas Oxisales 2. Obtener y nombrar en los tres sistemas los óxidos de: a. K b. Ba c. Sr d. N e. P f. S g. Cu h. Cl i. Br j. Al k. Cr l. C m. Mn n. Ni o. I p. F 3. Obtener y nombrar los hidróxidos a partir de los óxidos básicos (óxidos metálicos) obtenidos en el punto anterior 4. Obtener y nombrar en los tres sistemas los ácidos oxiácidos a partir de los óxidos ácidos (óxidos no metálicos) obtenidos en el punto 3. 5. Obtener y nombrar los ácidos hidrácidos de F, Cl, S, Br, I 6. Nombrar las sales que se obtengan de las siguientes reacciones: a. HCl + Sr(OH)2 → b. HNO3+ AgOH → c. H2 SO4 + KOH → d. H3 PO3 + Fe (OH)3→ e. H2 CO3 + KOH → f. HClO2 + Ni(OH)2 → g. H2 S + CuOH → h. HNO2 + Co(OH)3→ i. HIO + Pb(OH)4 → j. HBr + Cd(OH)2 →
- 3. PARTE II Completa la información de la tabla de acuerdo a las clases de nomenclatura. Siga los ejemplos: FORMULA N.STOCK N.SISTEMÁTICA (IUPAC) N.COMÚN F2O Óxido de flúor Óxido de diflúor Óxido de flúor I2O7 Óxido de yodo (VII) Heptóxido de diyodo Óxido periódico As2O5 CaO Fe2O3 PbO2 Al2O3 SnO N2O5 Au2O TeO2 Óxido áurico Óxido cuproso Óxido de selenio (II) Óxido crómico Óxido de platino (IV) Trihidróxido de aluminio Tetrahidróxido de plomo V2O5 Hidruro de cobalto (II) Ácido peryódico Fe(OH)3 Al(OH)3 B .Escribe la fórmula para cada uno de las siguientes sustancias: 1. Óxido de bario 2. Óxido de sodio 3. Óxido de plata 4. Óxido de aluminio 5. Óxido de níquel (III) 6. Óxido de cloro (VII) 7. Óxido nitroso 8. Óxido crómico 9. Hidruro de litio 10. Hidróxido de calcio 11. Hidruro de plata 12. Ácido brómico 13. Ácido sulfhídrico 14. Ácido clorhídrico 15. Óxido de bario 16. Hidruro de calcio 17. Óxido de sodio 18. Acido carbónico 19. Ácido clórico 20. Cloruro de sodio 21. Cloruro de calcio 22. Hidróxido ferroso 23. Ácido nitroso 24. Ácido sulfúrico 25. Ácido perclórico 26. Tricloruro de arsénico 27. Ácido perbrómico 28. Ácido Fosfórico 29. Nitrato de plata 30. Sulfuro de Zinc
