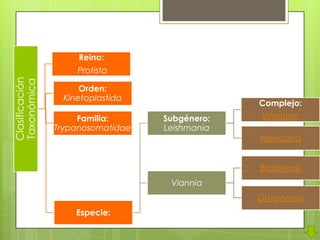
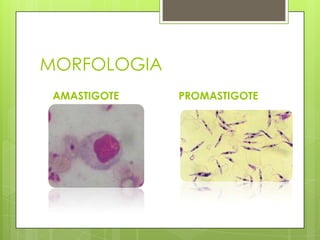
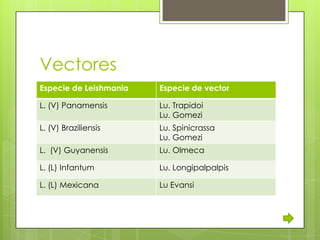
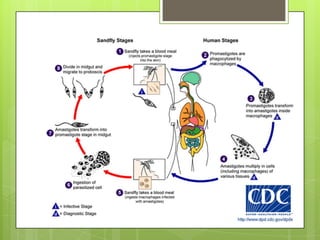
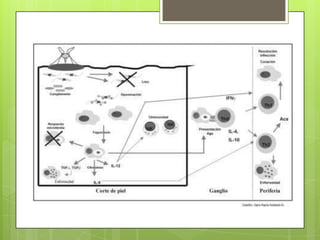
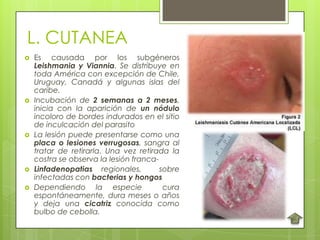
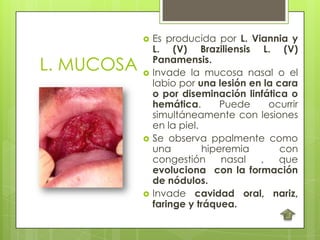
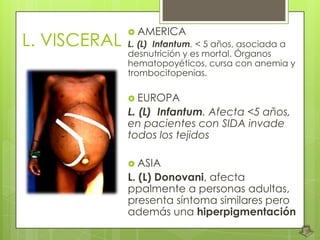
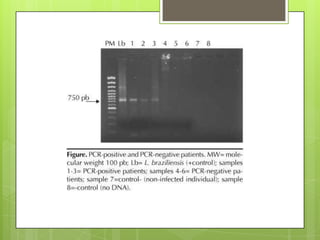
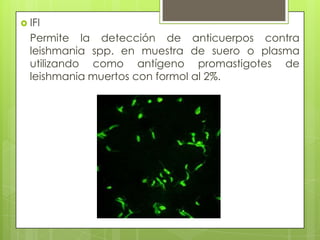
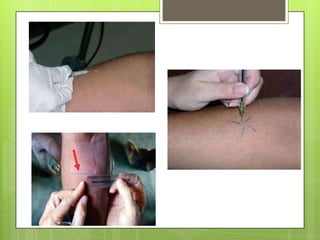
La leishmaniosis es una enfermedad parasitaria transmitida por la picadura de insectos flebotomos. Es causada por parásitos del género Leishmania que infectan mamíferos silvestres y domésticos. Existen distintas formas clínicas dependiendo del órgano afectado y la especie de Leishmania: cutánea, mucosa, difusa y visceral. Esta última afecta los órganos internos y es potencialmente mortal si no se trata.