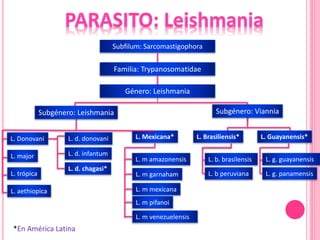
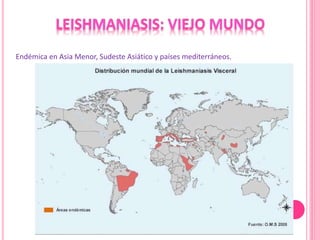
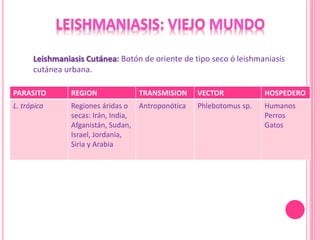
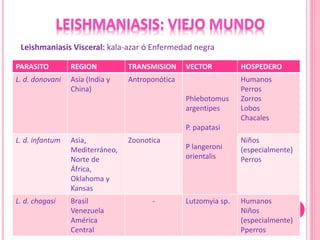
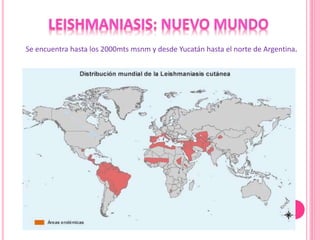
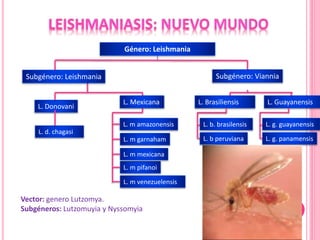
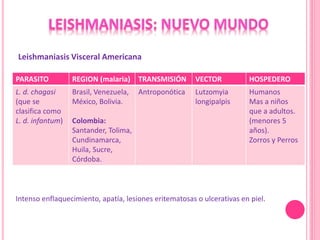
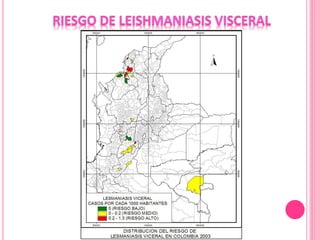
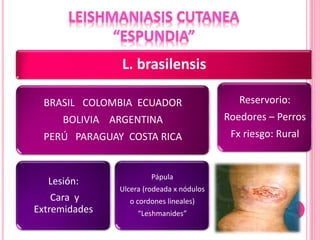
1. El documento describe las diferentes especies, regiones, vectores y hospederos de las principales formas de leishmaniasis.
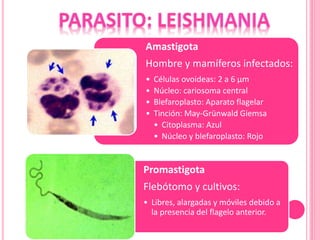
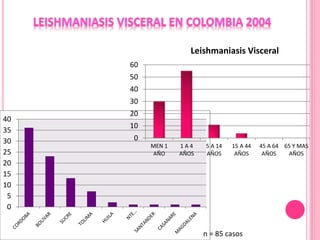
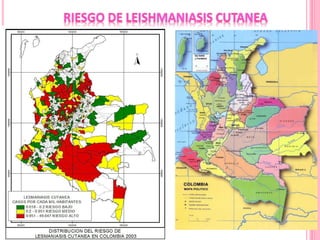
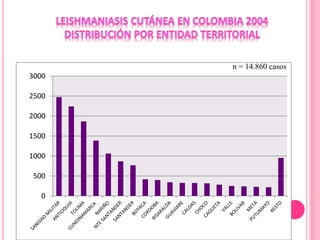
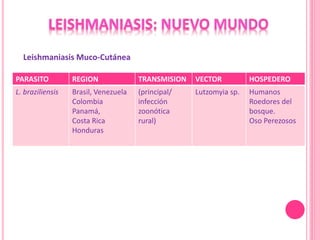
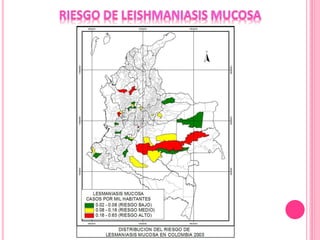
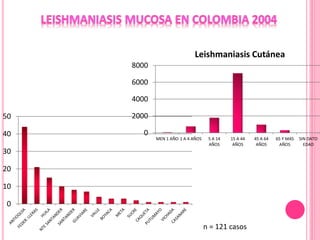
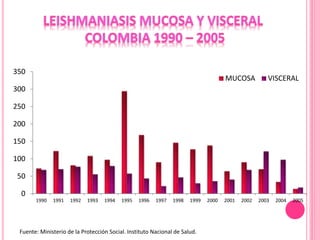
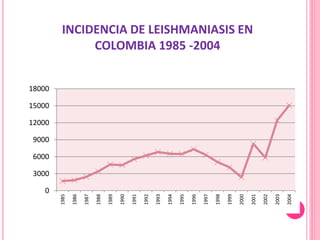
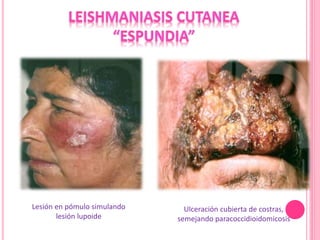
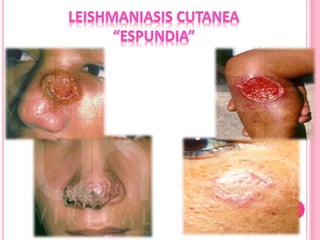
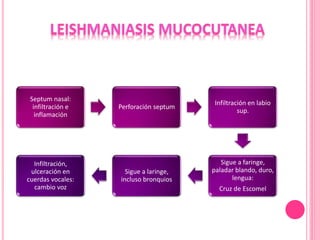
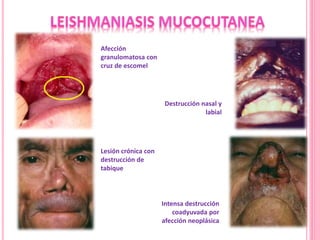
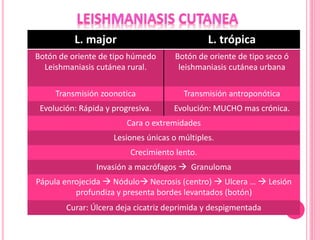
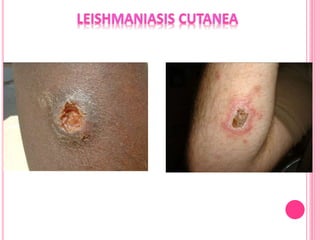
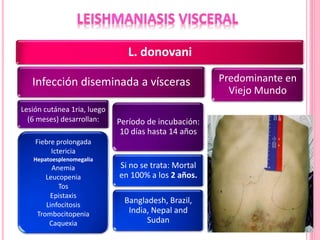
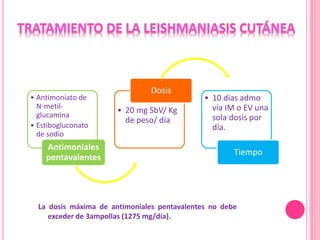
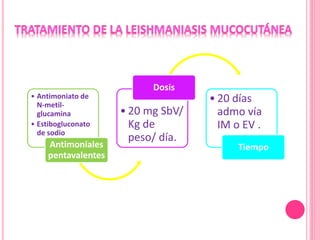
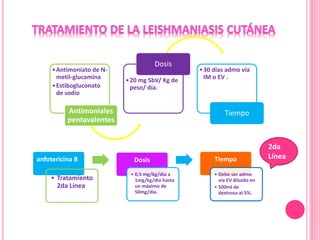
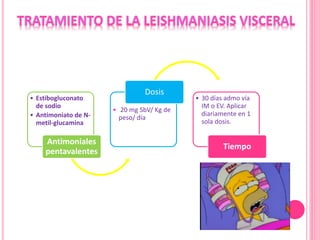
2. Se detallan las características clínicas de la leishmaniasis cutánea, mucocutánea y visceral producidas por distintas especies de Leishmania.
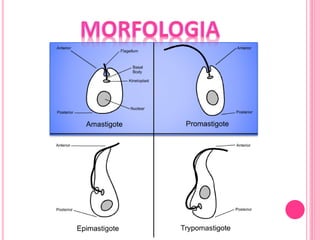
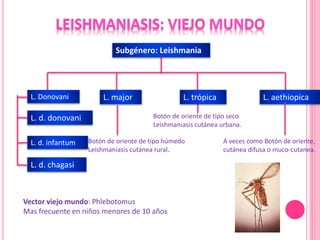
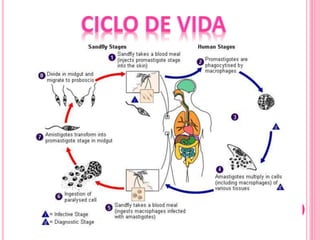
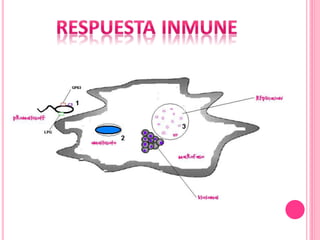
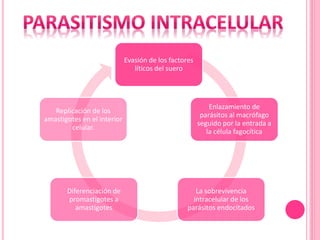
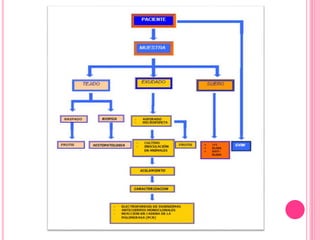
3. Se explica el ciclo de vida del parásito Leishmania y su transmisión entre vectores e hospederos humanos y animales.