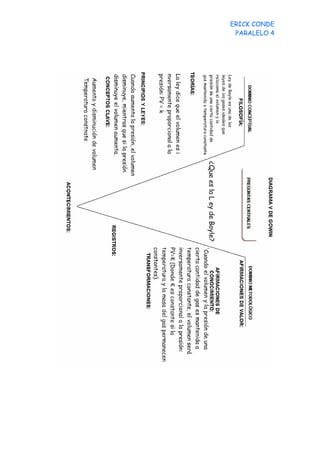
El documento describe un experimento para verificar la Ley de Boyle mediante la medición del volumen de un gas encerrado en un tubo en U a medida que se varía la presión aplicada. Se registraron 8 lecturas de volumen y presión, y los resultados muestran que a mayor presión, menor volumen, lo que confirma la relación inversa predicha por la ley de Boyle.



![ERICK CONDE
PARALELO 4
Cálculo para el volumen
Ø = (7.7 ± 0.1) X 10-3 m
V = πø² h ∆V = (πhø) ∆ø + πø² ∆h
4 2 4
V1 = πø² h1 ∆V1 = (πhø) ∆ø + πø² ∆h1
4 2 4
π π π
V1 = (7.7*10-3) 2(19.9*10-2) ∆V1 = (19.9*10-2)(7.7*10-3)(0.1*10-3) + (7.7*10-3) 2 (0.2*10-2)
4 2 4
V1 = 1.20*10-6 [m3] ∆V1 = 0.01*10-6 [m3]
V2 = πø² h2 ∆V2 = (πhø) ∆ø + πø² ∆h2
4 2 4
π π π
V2 = (7.7*10-3) 2 (20.2*10-2) ∆V2 = (20.2*10-2)(7.7*10-3)(0.1*10-3) + (7.7*10-3) 2 (0.2*10-2)
4 2 4
V2 = 1.22*10-6 [m3] ∆V2 = 0.01*10-6 [m3]
V3 = πø² h3 ∆V3 = (πhø) ∆ø + πø² ∆h3
4 2 4
π π π
V3 = (7.7*10-3) 2 (20.5*10-2) ∆V3 = (20.5*10-2)(7.7*10-3)(0.1*10-3) + (7.7*10-3) 2 (0.2*10-2)
4 2 4
V3 = 1.24*10-6 [m3] ∆V3 = 0.01*10-6 [m3]
V4 = πø² h4 ∆V4 = (πhø) ∆ø + πø² ∆h4
4 2 4
π π π
V4 = (7.7*10-3) 2 (20.8*10-2) ∆V4 = (20.8*10-2)(7.7*10-3)(0.1*10-3) + (7.7*10-3) 2 (0.2*10-2)
4 2 4
V4 = 1.26*10-6 [m3] ∆V4 = 0.01*10-6 [m3]
V5 = πø² h5 ∆V5 = (πhø) ∆ø + πø² ∆h5
4 2 4
π π π
V5 = (7.7*10-3) 2 (21.2*10-2) ∆V5 = (21.2*10-2)(7.7*10-3)(0.1*10-3) + (7.7*10-3) 2 (0.2*10-2)
4 2 4
V5 = 1.28*10-6 [m3] ∆V5 = 0.01*10-6 [m3]
V6 = πø² h6 ∆V6 = (πhø) ∆ø + πø² ∆h6](https://image.slidesharecdn.com/leydeboyle-100311213500-phpapp01/85/Ley-De-Boyle-4-320.jpg)
![ERICK CONDE
PARALELO 4
4 2 4
π π π
V6 = (7.7*10-3) 2 (21.7*10-2) ∆V6 = (21.7*10-2)(7.7*10-3)(0.1*10-3) + (7.7*10-3) 2 (0.2*10-2)
4 2 4
V6 = 1.31*10-6 [m3] ∆V6 = 0.01*10-6 [m3]
V7 = πø² h7 ∆V7 = (πhø) ∆ø + πø² ∆h7
4 2 4
π π π
V7 = (7.7*10-3) 2 (22.2*10-2) ∆V7 = (22.2*10-2)(7.7*10-3)(0.1*10-3) + (7.7*10-3) 2 (0.2*10-2)
4 2 4
V7 = 1.34*10-6 [m3] ∆V7 = 0.01*10-6 [m3]
V8 = πø² h8 ∆V8 = (πhø) ∆ø + πø² ∆h8
4 2 4
π π π
V8 = (7.7*10-3) 2 (28.8*10-2) ∆V8 = (28.8*10-2)(7.7*10-3)(0.1*10-3) + (7.7*10-3) 2 (0.2*10-2)
4 2 4
V8 = 1.74*10-6 [m3] ∆V8 = 0.01*10-6 [m3]
V´ = 1/V ∆V´= ∆V/ V 2
V1´ = 1/V1 ∆V1´= ∆V1 /(V1) 2
V1´ = 1/(1.20*10-6) ∆V1´= (0.01*10-6)/ (1.20*10-6) 2
V1´ = 8.33*105 [1/m3] ∆V1´= 0.01*105 [1/m3]
V2´ = 1/V2 ∆V2´= ∆V2 /(V2) 2
V2´ = 1/(1.22*10-6) ∆V2´= (0.01*10-6)/ (1.22*10-6) 2
V2´ = 8.19*105 [1/m3] ∆V2´= 0.01*105 [1/m3]
V3´ = 1/V3 ∆V3´= ∆V3 /(V3) 2
V3´ = 1/(1.24*10-6) ∆V3´= (0.01*10-6)/ (1.22*10-6) 2
V3´ = 8.06*105 [1/m3] ∆V3´= 0.01*105 [1/m3]
V4´ = 1/V4 ∆V4´= ∆V4 /(V4) 2
V4´ = 1/(1.26*10-6) ∆V4´= (0.01*10-6)/ (1.26*10-6) 2
V4´ = 7.93*105 [1/m3] ∆V4´= 0.01*105 [1/m3]
V5´ = 1/V5 ∆V5´= ∆V5 /(V5) 2
V5´ = 1/(1.28*10-6) ∆V5´= (0.01*10-6)/ (1.28*10-6) 2
V5´ = 7.81*105 [1/m3] ∆V5´= 0.01*105 [1/m3]
V6´ = 1/V6 ∆V6´= ∆V6 /(V6) 2](https://image.slidesharecdn.com/leydeboyle-100311213500-phpapp01/85/Ley-De-Boyle-5-320.jpg)
![ERICK CONDE
PARALELO 4
V6´ = 1/(1.31*10-6) ∆V6´= (0.01*10-6)/ (1.31*10-6) 2
V6´ = 7.63*105 [1/m3] ∆V6´= 0.01*105 [1/m3]
V7´ = 1/V7 ∆V7´= ∆V7 /(V7) 2
V7´ = 1/(1.34*10-6) ∆V7´= (0.01*10-6)/ (1.34*10-6) 2
V7´ = 7.46*105 [1/m3] ∆V7´= 0.01*105 [1/m3]
V8´ = 1/V8 ∆V8´= ∆V8 /(V8) 2
V8´ = 1/(1.74*10-6) ∆V8´= (0.01*10-6)/ (1.74*10-6) 2
V8´ = 5.75*105 [1/m3] ∆V8´= 0.01*105 [1/m3]
Cálculo de la presión del gas
PO = (1.01 ± 0.01)*105 pa g = (9.81 ± 0.01) m/s2
ρhg = (13.55 ± 0.01)*103 kg/m3
Pgas = P0 – ρhg g H ∆Pgas = ∆P0 + gH∆ρhg + ρhgH∆g + ρhg g∆H
P1 gas = P0 – ρhg g H1
P1 gas = (1.01*105) – (13.55*103)(9.81)(1.0*10-2)
P1 gas = 9.97*104 [N/m2]
∆P1 gas = ∆P0 + gH1∆ρhg + ρhgH1∆g + ρhg g∆H1
∆P1 gas = (0.01*105) + (9.81*1.0*10-2)(0.01*103) + (13.55*103)*(1.0*10-2)*(0.01) + (13.55*103)*(9.81)*(0.02*10-2)
∆P1 gas = 0.01*10 [N/m ]
4 2
P2 gas = P0 – ρhg g H2
P2 gas = (1.01*10 ) – (13.55*10 )(9.81)(1.8*10 )
5 3 -2
P2 gas = 9.86*10 [N/m ]
4 2
∆P2 gas = ∆P0 + gH2∆ρhg + ρhgH2∆g + ρhg g∆H2
∆P2 gas = (0.01*10 ) + (9.81*1.8*10 )(0.01*10 ) + (13.55*10 )*(1.8*10 )*(0.01) + (13.55*10 )*(9.81)*(0.02*10 )
5 -2 3 3 -2 3 -2
∆P2 gas = 0.01*10 [N/m ]
4 2
P3 gas = P0 – ρhg g H3
P3 gas = (1.01*105) – (13.55*103)(9.81)(2.6*10-2)
P3 gas = 9.75*10 [N/m ]
4 2
∆P3 gas = ∆P0 + gH3∆ρhg + ρhgH3∆g + ρhg g∆H3
∆P3 gas = (0.01*105) + (9.81*2.6*10-2)(0.01*103) + (13.55*103)*(2.6*10-2)*(0.01) + (13.55*103)*(9.81)*(0.02*10-2)
∆P3 gas = 0.01*10 [N/m ]
4 2
P4 gas = P0 – ρhg g H4](https://image.slidesharecdn.com/leydeboyle-100311213500-phpapp01/85/Ley-De-Boyle-6-320.jpg)
![ERICK CONDE
PARALELO 4
P4 gas = (1.01*105) – (13.55*103)(9.81)(3.1*10-2)
P4 gas = 9.69*10 [N/m ]
4 2
∆P4 gas = ∆P0 + gH4∆ρhg + ρhgH4∆g + ρhg g∆H4
∆P4 gas = (0.01*10 ) + (9.81*3.1*10 )(0.01*10 ) + (13.55*10 )*(3.1*10 )*(0.01) + (13.55*10 )*(9.81)*(0.02*10 )
5 -2 3 3 -2 3 -2
∆P4 gas = 0.01*10 [N/m ]
4 2
P5 gas = P0 – ρhg g H5
P5 gas = (1.01*10 ) – (13.55*10 )(9.81)(3.6*10 )
5 3 -2
P5 gas = 9.62*10 [N/m ]
4 2
∆P5 gas = ∆P0 + gH5∆ρhg + ρhgH5∆g + ρhg g∆H5
∆P5 gas = (0.01*10 ) + (9.81*3.6*10 )(0.01*10 ) + (13.55*10 )*(3.6*10 )*(0.01) + (13.55*10 )*(9.81)*(0.02*10 )
5 -2 3 3 -2 3 -2
∆P5 gas = 0.01*10 [N/m ]
4 2
P6 gas = P0 – ρhg g H6
P6 gas = (1.01*10 ) – (13.55*10 )(9.81)(4.3*10 )
5 3 -2
P6 gas = 9.53*10 [N/m ]
4 2
∆P6 gas = ∆P0 + gH6∆ρhg + ρhgH6∆g + ρhg g∆H6
∆P6 gas = (0.01*10 ) + (9.81*4.3*10 )(0.01*10 ) + (13.55*10 )*(4.3*10 )*(0.01) + (13.55*10 )*(9.81)*(0.02*10 )
5 -2 3 3 -2 3 -2
∆P6 gas = 0.01*10 [N/m ]
4 2
P7 gas = P0 – ρhg g H7
P7 gas = (1.01*105) – (13.55*103)(9.81)(4.7*10-2)
P7 gas = 9.46*10 [N/m ]
4 2
∆P7 gas = ∆P0 + gH7∆ρhg + ρhgH7∆g + ρhg g∆H7
∆P7 gas = (0.01*105) + (9.81*4.7*10-2)(0.01*103) + (13.55*103)*(4.7*10-2)*(0.01) + (13.55*103)*(9.81)*(0.02*10-2)
∆P7 gas = 0.01*10 [N/m ]
4 2
P8 gas = P0 – ρhg g H8
P8 gas = (1.01*105) – (13.55*103)(9.81)(5.7*10-2)
P8 gas = 9.34*10 [N/m ]
4 2
∆P8 gas = ∆P0 + gH8∆ρhg + ρhgH8∆g + ρhg g∆H8
∆P8 gas = (0.01*105) + (9.81*5.7*10-2)(0.01*103) + (13.55*103)*(5.7*10-2)*(0.01) + (13.55*103)*(9.81)*(0.02*10-2)
∆P8 gas = 0.01*10 [N/m ]
4 2](https://image.slidesharecdn.com/leydeboyle-100311213500-phpapp01/85/Ley-De-Boyle-7-320.jpg)
![ERICK CONDE
PARALELO 4
TABLA DE DATOS
H Pgas h V 1/V
(*10-2 m) (*104 N/m2) (*10-2 m) (*10-6 m3) (*105 /m3)
1.0 ± 0.2 9.97 ± 0.01 19.9 ± 0.2 1.20 ± 0.01 8.33 ± 0.01
1.8 ± 0.2 9.86 ± 0.01 20.2 ± 0.2 1.22 ± 0.01 8.19 ± 0.01
2.6 ± 0.2 9.75 ± 0.01 20.5 ± 0.2 1.24 ± 0.01 8.06 ± 0.01
3.1 ± 0.2 9.69 ± 0.01 20.8 ± 0.2 1.26 ± 0.01 7.93 ± 0.01
3.6 ± 0.2 9.62 ± 0.01 21.2 ± 0.2 1.28 ± 0.01 7.81 ± 0.01
4.3 ± 0.2 9.53 ± 0.01 21.7 ± 0.2 1.31 ± 0.01 7.63 ± 0.01
4.7 ± 0.2 9.46 ± 0.01 22.2 ± 0.2 1.34 ± 0.01 7.46 ± 0.01
5.7 ± 0.2 9.34 ± 0.01 28.8 ± 0.2 1.74 ± 0.01 5.75 ± 0.01
CÁLCULO DE LA PENDIENTE
P1 = ( [7.60 ± 0.01] * 105 1/m3 , [9.50 ± 0.01] * 104 N/m2 )
P2 = ( [9.05 ± 0.01] * 105 1/m3 , [10.40 ± 0.01] * 104 N/m2 )
a = y 2 – y1 ∆a = ∆y2 + ∆y1
a = (10.40 –9.50)*104 N/m2 ∆a = (0.01 + 0.01) *104 N/m2
a = 0.90*104 N/m2 ∆a = 0.02*104 N/m2
b = x 2 – x1 ∆b = ∆x2 + ∆x1
b = (9.05 – 7.60)*105 1/m3 ∆b = (0.01 + 0.01)*105 1/m3
b = 1.45 *105 1/m3 ∆b = 0.02*105 1/m3
m=a/b ∆m = (b a∆ + a ∆b) / b²
m = 0.90*104/1.45 *105 ∆m=[(1.45*10 5
*0.02*104)+(0.90*104 *0.02*105)]/( 1.45 *105 )²
m = 0.62*10-1 N/m ∆m = 0.02*10-1 N/m
m = (0.62 ± 0.02) *10-1 N/m](https://image.slidesharecdn.com/leydeboyle-100311213500-phpapp01/85/Ley-De-Boyle-8-320.jpg)