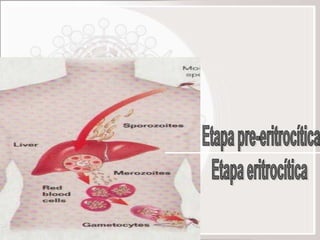
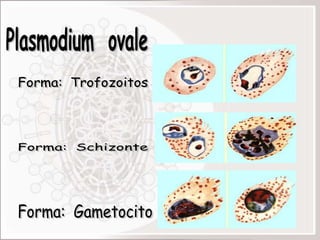
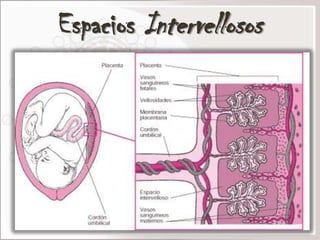
La malaria en el embarazo puede causar complicaciones graves tanto para la madre como para el feto. La infección se produce cuando la hembra Anopheles infectada transmite esporozoitos al picar a la mujer embarazada. Los parásitos invaden los eritrocitos y se adhieren a la placenta, lo que puede provocar anemia, bajo peso al nacer, e incluso la muerte del feto o la madre. Es importante el diagnóstico y tratamiento oportunos de la malaria durante el embarazo para prevenir estas complicaciones.