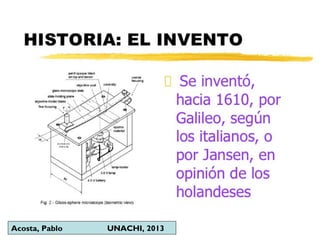
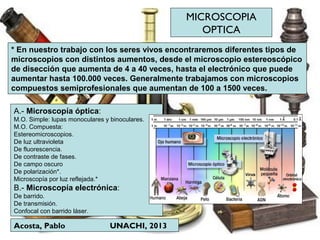
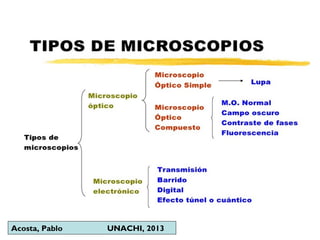
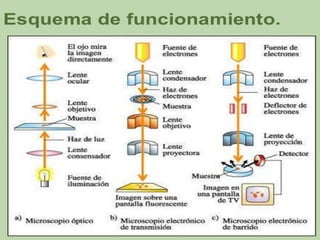
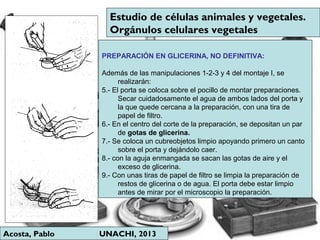
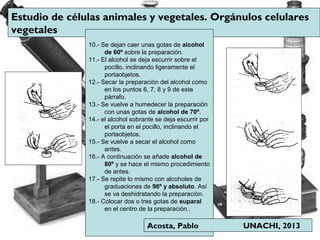
Este documento describe los procedimientos para la preparación y montaje de muestras biológicas para su examen bajo microscopía óptica. Explica los diferentes tipos de microscopios, incluidos los microscopios ópticos simples y compuestos y los microscopios electrónicos. Luego detalla los pasos para preparar muestras tanto in vivo como in vitro, incluida la fijación, inclusión, corte y tinción de tejidos. Finalmente, proporciona instrucciones detalladas para realizar cortes con un micro