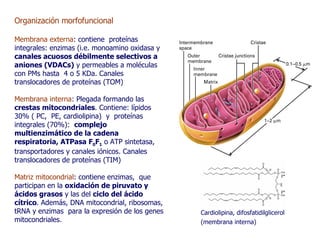
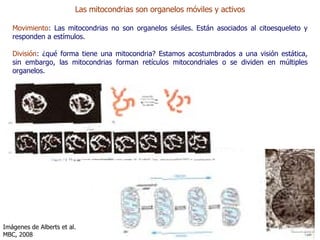
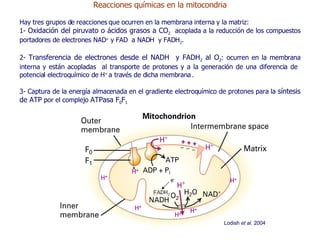
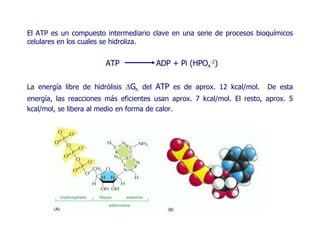
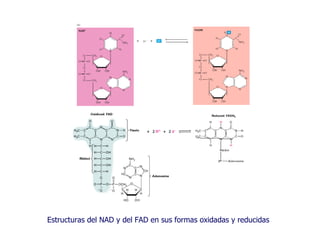
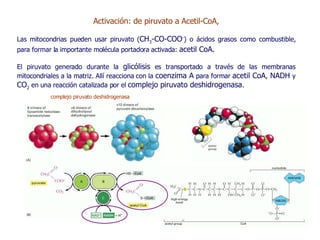
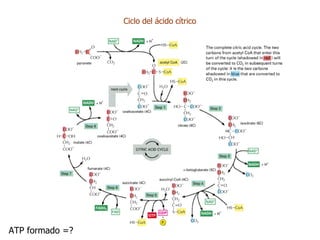
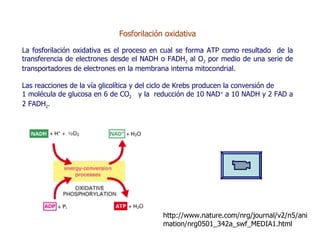
Este documento resume las funciones y características de las mitocondrias en 3 oraciones. Las mitocondrias son organelos que producen ATP a través de reacciones de óxido-reducción en las cuales se transportan electrones para generar un gradiente de protones y fosforilar ADP. Contienen dos membranas y DNA mitocondrial. Las reacciones en la matriz y membrana interna incluyen la oxidación de piruvato y ácidos grasos para reducir NAD+ y FAD, y la fosforilación oxidativa para sintetizar