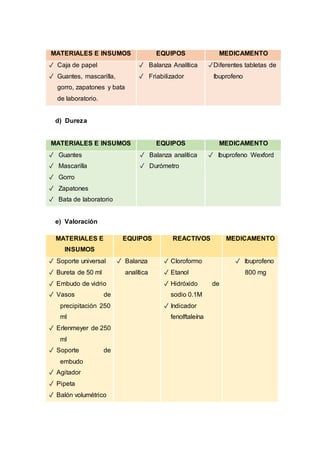
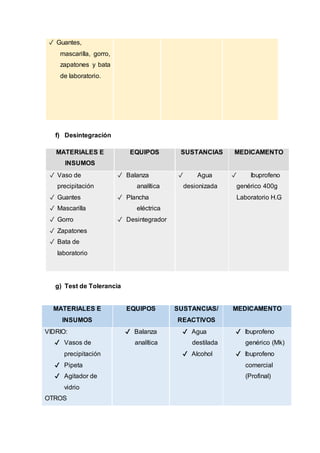
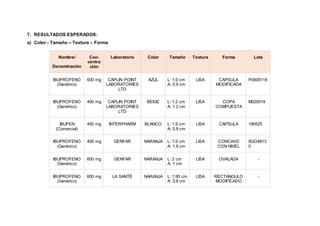
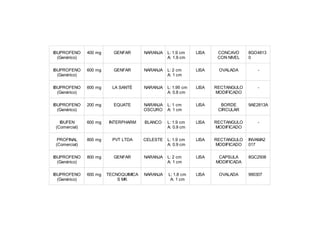
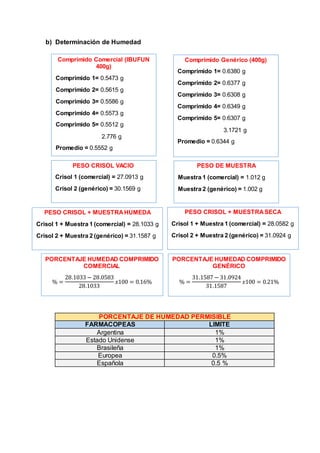
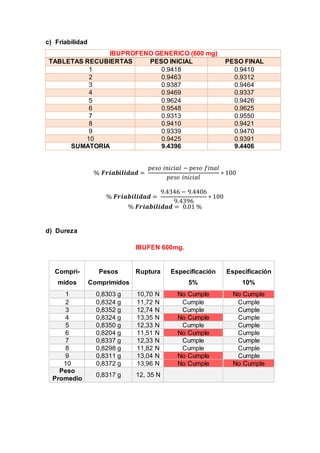
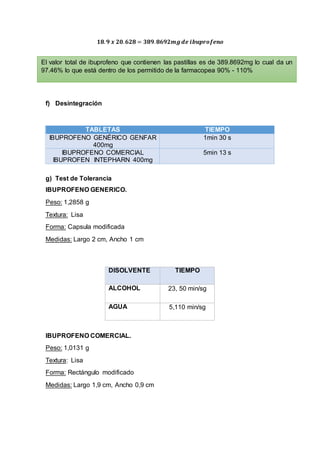
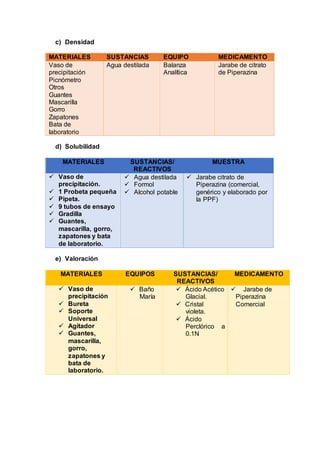
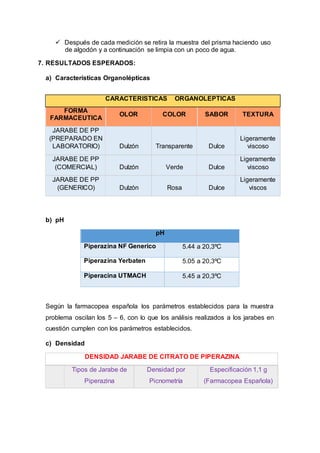
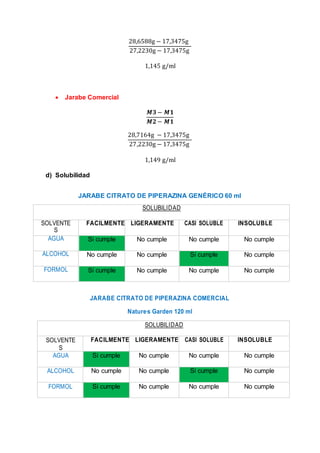
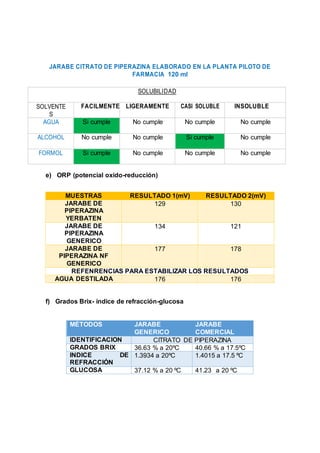
Este documento describe un procedimiento de laboratorio para evaluar la calidad de un medicamento de ibuprofeno. Se realizarán pruebas para determinar el color, tamaño, textura y forma de comprimidos genéricos y comerciales de ibuprofeno, así como su humedad, friabilidad, dureza y contenido de principio activo. El objetivo es comprobar si los medicamentos cumplen con los parámetros establecidos en la farmacopea. Se espera que los resultados proporcionen información sobre las características físicas y qu