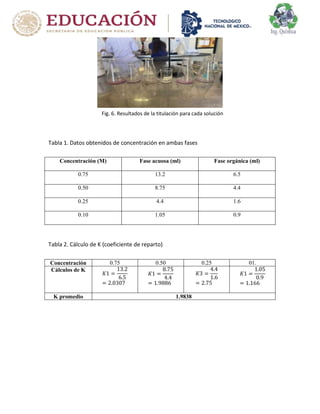
El documento describe un experimento para determinar el coeficiente de reparto del ácido acético entre agua y éter etílico usando la Ley de Nernst. Se prepararon cuatro soluciones con diferentes concentraciones de ácido acético y se agitaron con éter etílico. Las capas se separaron y titularon para calcular el coeficiente de reparto, el cual promedio fue de 1.9835, similar pero no igual al valor teórico debido a posibles variaciones experimentales.




![Nx (X) n
CB (1- α) CB(
𝑎
𝑛
)
Donde α es el grado de asociación y n es el número de moléculas de soluto que se combinan
para formar una molécula asociada (X)n. Aplicando la ley de la acción de masa en el
equilibrio anterior se tiene que:
K=
𝐶𝐵(
∝
𝑛
)
[𝐶𝐵(1−𝑛)]𝑛
O
𝐶𝐵(1 − 𝑛)]𝑛
= (
∝𝐶𝐵
𝑛𝐾
)
𝐶𝐵(1 − 𝑛)] = (
∝𝐶𝐵
𝑛𝐾
)
1
𝑛
Entonces la constante de distribución está dada por:
K =
𝐶𝐴
𝐶𝐵(1−𝑛)
K =
𝐶𝐴
(
∝𝐶𝐵
𝑛𝐾
)
1
𝑛
K =
𝐶𝐴
𝐶𝐵
1
𝑛
(
𝑛𝐾
∝
)
1
𝑛
Como K y α son constantes y dependen sólo de la temperatura, entonces a temperaturas
constante, la cantidad Nk/ α es una constante, y la ecuación anterior se convierte en:
K = constante
𝐶𝐴
𝐶𝐵
1/𝑛](https://image.slidesharecdn.com/prctica4-221116182807-93d34984/85/Practica-4-Ley-de-Nernst-docx-5-320.jpg)