El documento presenta un examen de química dividido en dos niveles (A y B) que contiene 41 preguntas de opción múltiple sobre diversos temas de química como propiedades intensivas y extensivas, enlaces químicos, estequiometría, equilibrio químico, ácidos y bases, termoquímica y electroquímica. El examen busca evaluar los conocimientos químicos básicos de los estudiantes.



![a) fundir benceno
b) hervir agua
c) electrolisis del agua
d) hervir etanol
20.- Un refresco embotellado con una presión de dióxido de carbono de 2.2 atm. Que
fracción de CO2 se libera al abrir la botella si la presión baja hasta 0.010 atm?
a) 1.550
b) 0.550
c) 0.950
d) 0.995
21.- Seleccione la constante de equilibrio para el siguiente sistema
O2(g) + 4 HCl(g) 2 H2O(g) + 2 Cl2(g)
a) [H2O][Cl]2/[O2] 4[HCl]
b) 2[H2O][Cl]2/[O2]2 4[HCl]
c) [H2O]2[Cl2]2/[O2][HCl]4
d) 2[H2O]2 2[Cl2]2/[O2] 4[HCl]4
22.- Cual es el tipo más importante de fuerzas atractivas que hay que vencer para vaporizar
NH3(l).
a) dispersión
b) enlace covalente
c) enlace iónico
d) enlaces de H
23.- Una disolución saturada de BaF2 contiene 1.38 g/L. Calcular el Ks del BaF2.
a) 1.95 x 10-6
b) 7.87 x 10-3
c) 1.9 x 10-3
d) 2 x 10-6
24.- Considere estos ácidos
Acido
A
B
C
D pKa
ordene los ácidos en sentido creciente de acidez.
a) A<C<B<D
b) D<A<B<C
c) D<B<A<C
d) B<D<A<C
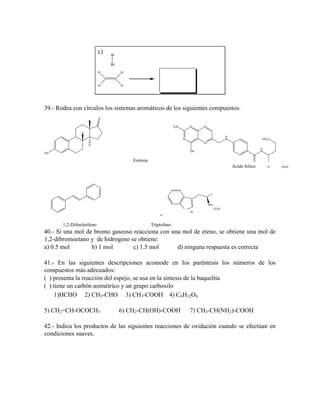
6.8
4.4
1.9
11.2](https://image.slidesharecdn.com/9-140121210627-phpapp01/85/PROBLEMAS-DE-QUIMICA-GENERAL-4-320.jpg)
![25.- Calcula la [H+] y el pH de un tampón preparado añadiendo 0.030 moles de H2PO4- a
3.00 L de una solución 0.020 M de HPO4-2.
a) 3.9 x 10-7 M
pH=7.31
-8
b) 3.45 x 10 M pH=7.4
c) 3.1 x 10-8 M pH=7.51
d) 4 x 10-7 M
pH=7.2
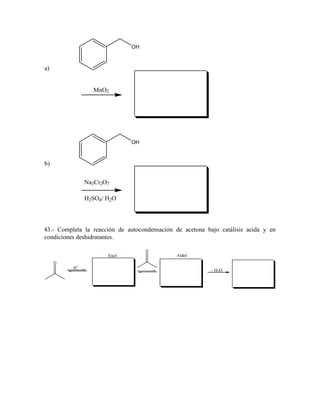
26.- Cuales son los coeficientes estequiometricos de la siguiente reacción redox: I+ MnO4- + H2O
I2 + MnO2 + OH27.- El pH de una solución 0.01 M en HY es de 2.40. Cuál es el valor de la Ka del HY?
a) 4.0 x 10-3
b) 2.4 x 10-3
c) 1.6 x 10-3
d) 2.7 x 10-3
28.- Cual es la concentración molar de KMnO4 en una solución que se preparo al disolver
47.4 g de KMnO4 en aproximadamente 500 mL de agua y al diluirla luego a 5 L?
a) 6.00 x 10-2
b) 6.67 x 10-1 M
c) 5.45 x 10-2 M
d) 6 x 10-4 M
29.- -----30.- Si se establece el equilibrio de P4(g) + 6 Cl2(g) 4 PCl3(g) agregando igual número
de moles de P4 y Cl2 en un matraz vacio. Cuáles de las siguientes afirmaciones son
verdaderas en estado de equilibrio?
a) [Cl2]>[PCl3]
b) [Cl2]>[P4]
c) [P4]>[Cl2]
d) [PCl3]>[P4]
HASTA AQUÍ NIVEL B
31.- En electroquímica se utiliza mucho la constante de Faraday que equivale a:
a) El potencial del electrodo de hidrogeno
b) El potencial del electrodo en el vacio
c) La corriente de un circuito que tiene la capacidad de un Faraday
d) La carga de una mol de electrones
32.- La unidad de potencial eléctrica es el:
a) watt
b) ampere
c) coulomb
d) Faraday](https://image.slidesharecdn.com/9-140121210627-phpapp01/85/PROBLEMAS-DE-QUIMICA-GENERAL-5-320.jpg)