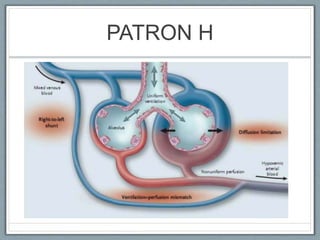
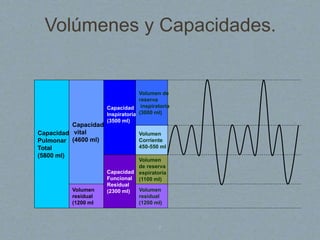
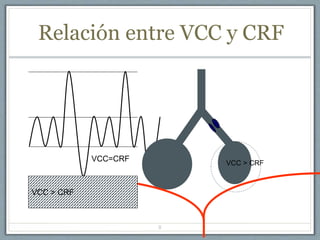
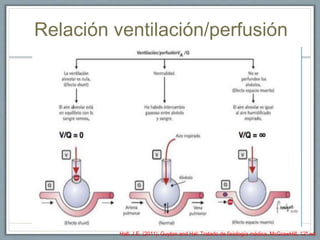
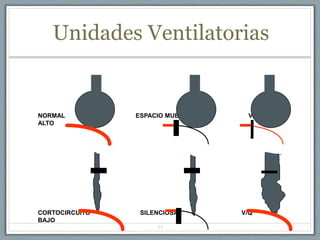
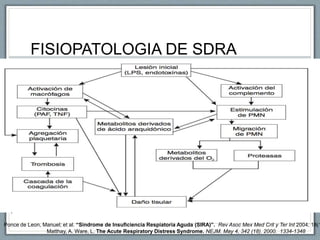
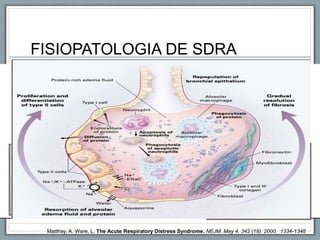
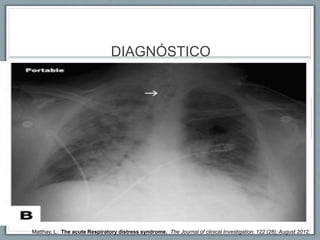
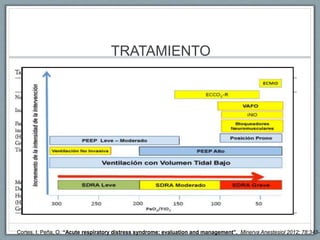
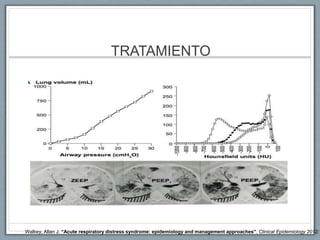
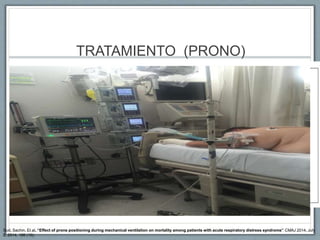
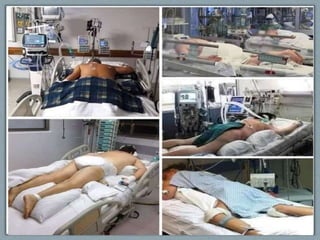
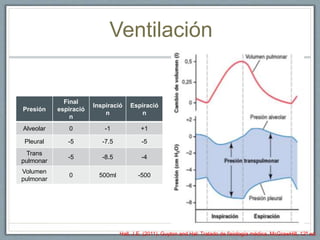
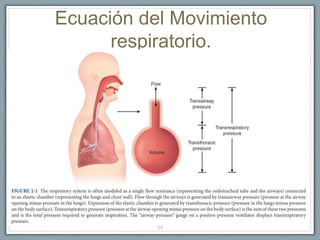
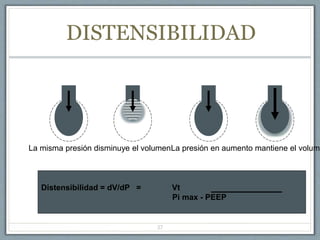
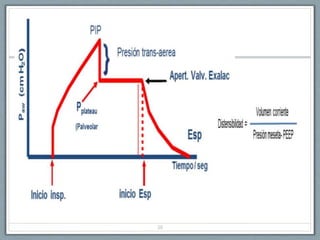
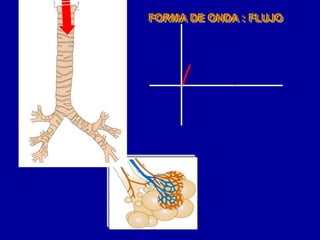
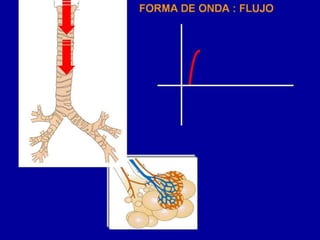
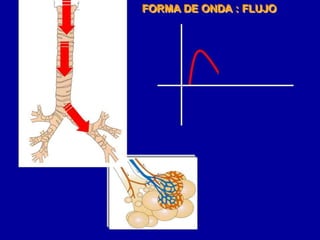
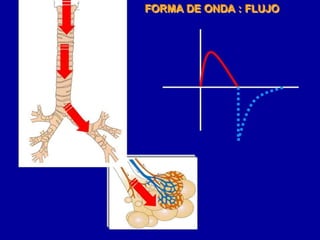
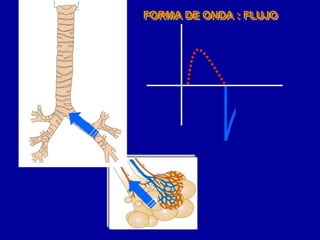
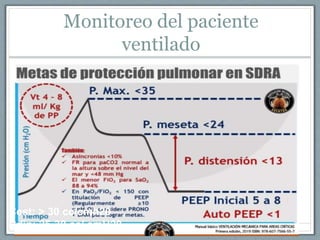
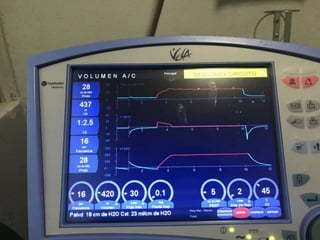
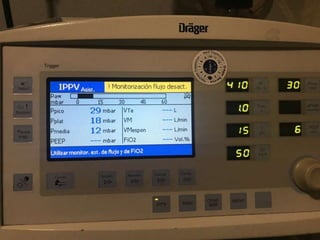
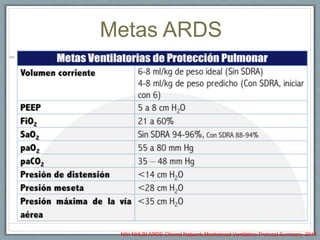
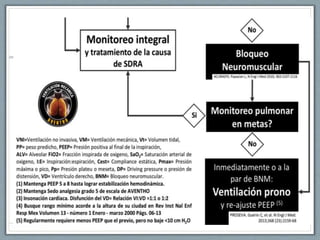
El documento proporciona información sobre la ventilación mecánica y el manejo de pacientes con COVID-19. Describe dos patrones pulmonares (patrón L y patrón H), volúmenes y capacidades pulmonares, y la relación ventilación/perfusión. También resume las características de la insuficiencia respiratoria aguda, la fisiopatología del síndrome de distrés respiratorio agudo, el cuadro clínico, diagnóstico y tratamiento incluyendo soporte ventilatorio y pronación.