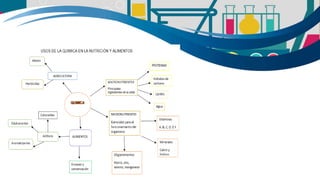
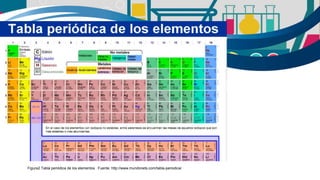
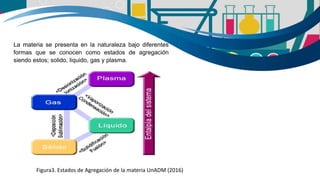
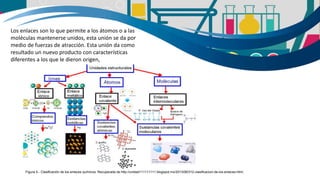
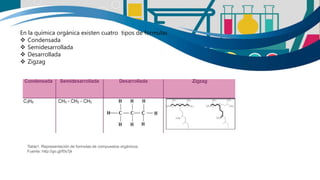
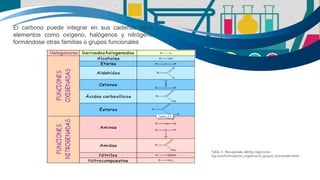
La química es fundamental para la vida y se encuentra en todos los aspectos de nuestra existencia. Está presente en los procesos metabólicos de los organismos vivos y en la transformación de los alimentos. La química se divide en química general, química descriptiva orgánica e inorgánica. La tabla periódica es una herramienta clave para estudiar la química al mostrar las propiedades de los elementos. Los compuestos orgánicos se encuentran en toda la naturaleza y son importantes para la vida.