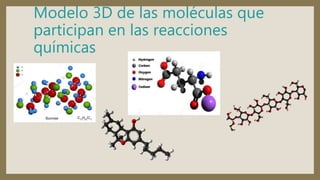
Este documento describe varias técnicas para prevenir la corrosión de los metales, incluyendo el uso de acero inoxidable, recubrimientos de zinc, pinturas especiales y ánodos de zinc. Explica que científicos del Cinvestav han desarrollado recubrimientos ultradelgados de materiales nanoestructurados que protegen partes metálicas expuestas a altas temperaturas. También presenta experimentos para identificar ácidos y bases usando indicadores de pH.