Incrustar presentación
Descargado 134 veces

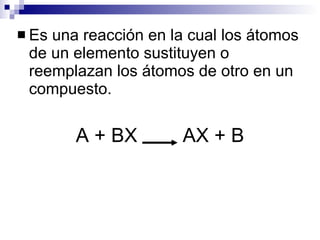








Este documento describe las reacciones de desplazamiento o sustitución, donde los átomos de un elemento reemplazan a los de otro en un compuesto. Explica cómo los metales desplazan átomos de hidrógeno del agua o ácidos, y cómo los metales más reactivos pueden desplazar a otros metales menos reactivos en sales. También describe cómo los halógenos más reactivos pueden reemplazar a otros halógenos menos reactivos. La capacidad de una sustancia para reaccionar de esta manera se conoce como su









