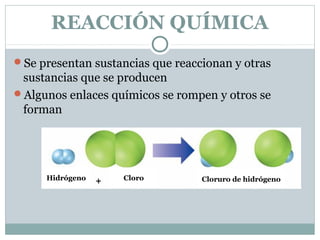
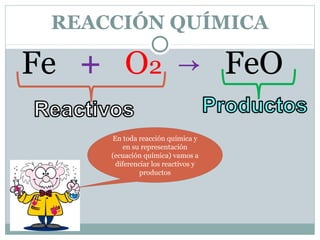
Una reacción química es un proceso en el que los reactivos se transforman en productos mediante el rompimiento y formación de enlaces químicos, manteniendo la masa constante. Se pueden identificar por cambios como color, formación de gas o precipitado, y transferencia de energía. La ley de conservación de la masa establece que la masa total antes y después de la reacción es la misma, y es esencial balancear las ecuaciones químicas para reflejar esto.