Sistema etanol agua l v
•
0 recomendaciones•5,830 vistas
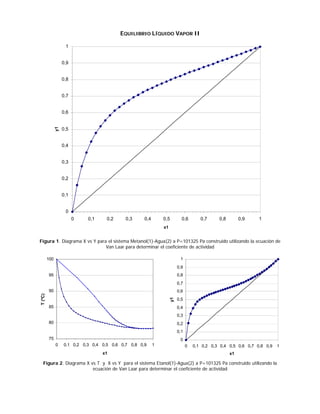
El documento presenta dos figuras que muestran diagramas de equilibrio líquido-vapor para sistemas binarios de metanol-agua y etanol-agua. La Figura 1 muestra un diagrama X vs Y a 101325 Pa para metanol-agua, construido usando la ecuación de Van Laar. La Figura 2 presenta diagramas X vs T y X vs Y para etanol-agua a la misma presión, también usando Van Laar.
Denunciar
Compartir
Denunciar
Compartir
Descargar para leer sin conexión
Recomendados
Guia resuelta de destilación fraccionada

Si todos los componentes del sistema se distribuyen entre las fases en el equilibrio, la operación se conoce como destilación fraccionada (o con frecuencia, simplemente como destilación).
Problemas transferencia de materia

Ley de Fick, Difusión equimolar en estado estacionario. Difusividad de gases. Calculo del flujo difusional. Problemas resueltos de transferencia de materia.
Documents.tips solucionario geankoplis-procesos-de-transporte-y-operaciones-u...

este ayuda a las soluciones de geankoplis que pueden ser difíciles para ti.
comprender que todos los problemas planteados en el libro de geankoplis esta en este solucionario.
debes comprender que el solucionario es ayuda para los ejercisios lo de mas depende de como desarrolles tus habilidades .
Problema n°1 Destilación Flash.pdf

Problema de destilación Flash resuelto paso a paso, de operaciones unitaria I de ingeniería química, del Geankoplis
Recomendados
Guia resuelta de destilación fraccionada

Si todos los componentes del sistema se distribuyen entre las fases en el equilibrio, la operación se conoce como destilación fraccionada (o con frecuencia, simplemente como destilación).
Problemas transferencia de materia

Ley de Fick, Difusión equimolar en estado estacionario. Difusividad de gases. Calculo del flujo difusional. Problemas resueltos de transferencia de materia.
Documents.tips solucionario geankoplis-procesos-de-transporte-y-operaciones-u...

este ayuda a las soluciones de geankoplis que pueden ser difíciles para ti.
comprender que todos los problemas planteados en el libro de geankoplis esta en este solucionario.
debes comprender que el solucionario es ayuda para los ejercisios lo de mas depende de como desarrolles tus habilidades .
Problema n°1 Destilación Flash.pdf

Problema de destilación Flash resuelto paso a paso, de operaciones unitaria I de ingeniería química, del Geankoplis
Guia resuelta de destilación

La destilación es un método que se usa para separar los componentes de una solución líquida, el cual depende de la distribución de estos componentes entre una fase de vapor y una fase líquida. Ambos componentes están presentes en las dos fases. La fase de vapor se origina de la fase líquida por vaporización en el punto de ebullición
Thermodynamics of solutions. Solved problems (Spanish)

Solved problems of partial properties, excess and residual properties and fugacities.
Equipo para extracción líquido líquido

Se describen los principales tipos de equipos utilizados en la operación de extracción líquido-líquido.
Tipos y equipos de evaporadores

Tipos, equipos de evaporadores, métodos de operación.
Efecto simple y multiple.
Coeficientes totales de transferencia de calor en evaporadores
Más contenido relacionado
La actualidad más candente
Guia resuelta de destilación

La destilación es un método que se usa para separar los componentes de una solución líquida, el cual depende de la distribución de estos componentes entre una fase de vapor y una fase líquida. Ambos componentes están presentes en las dos fases. La fase de vapor se origina de la fase líquida por vaporización en el punto de ebullición
Thermodynamics of solutions. Solved problems (Spanish)

Solved problems of partial properties, excess and residual properties and fugacities.
Equipo para extracción líquido líquido

Se describen los principales tipos de equipos utilizados en la operación de extracción líquido-líquido.
Tipos y equipos de evaporadores

Tipos, equipos de evaporadores, métodos de operación.
Efecto simple y multiple.
Coeficientes totales de transferencia de calor en evaporadores
La actualidad más candente (20)
Thermodynamics of solutions. Solved problems (Spanish)

Thermodynamics of solutions. Solved problems (Spanish)
Mendoza ventura jesus balance de materia y energia cristalizacion

Mendoza ventura jesus balance de materia y energia cristalizacion
Criterios para la seleccion de equipos de cristalizacion

Criterios para la seleccion de equipos de cristalizacion
Destacado
Destacado (11)
Sustancias Puras, Gases Ideales, Diagrama De Propiedades

Sustancias Puras, Gases Ideales, Diagrama De Propiedades
Similar a Sistema etanol agua l v
Similar a Sistema etanol agua l v (11)
Sistema etanol agua l v
- 1. EQUILIBRIO LÍQUIDO VAPOR II 1 0,9 0,8 0,7 0,6 y1 0,5 0,4 0,3 0,2 0,1 0 0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 0,9 1 x1 Figura 1. Diagrama X vs Y para el sistema Metanol(1)-Agua(2) a P=101325 Pa construido utilizando la ecuación de Van Laar para determinar el coeficiente de actividad 100 1 0,9 95 0,8 0,7 90 0,6 T (ºC) y1 0,5 85 0,4 0,3 80 0,2 0,1 75 0 0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 0,9 1 0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 0,9 1 x1 x1 Figura 2. Diagrama X vs T y X vs Y para el sistema Etanol(1)-Agua(2) a P=101325 Pa construido utilizando la ecuación de Van Laar para determinar el coeficiente de actividad