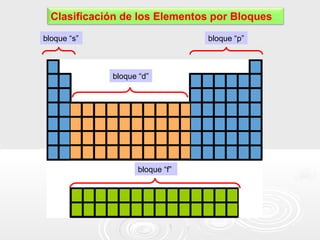
El documento resume la tabla periódica actual de los elementos. Explica que los 112 elementos reconocidos están ordenados por número atómico creciente en 7 períodos y 16 grupos. Los períodos indican la estructura atómica de los elementos y los grupos sus propiedades químicas similares. Además, clasifica los elementos como metales, no metales y semimetales según sus propiedades físicas y químicas.