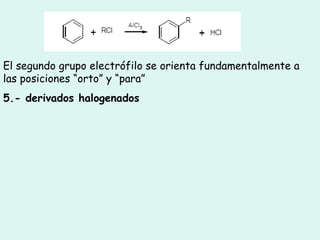
El documento proporciona información sobre compuestos orgánicos. Explica que el carbono puede formar enlaces con otros elementos debido a su electronegatividad e hidrocarburos. Describe los tipos de isomería y reacciones que ocurren en compuestos orgánicos, incluidas sustitución, adición y eliminación. También clasifica hidrocarburos como alcanos y alquenos.




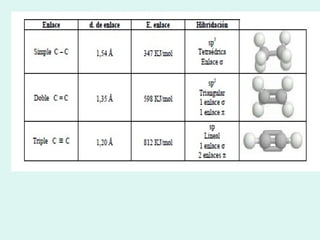

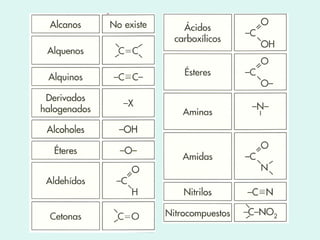
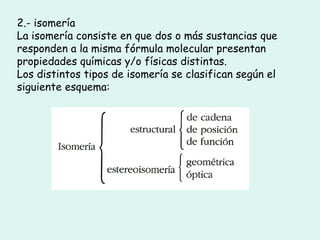

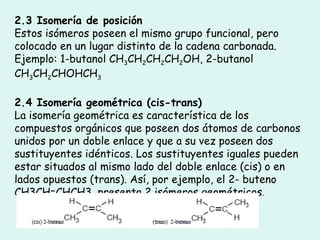








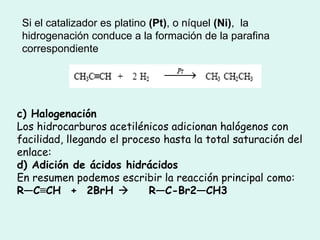
![4 .2 Alcanos o parafinas Recordemos que se llama parafinas o hidrocarburos saturados a aquellos que se caracterizan por presentar exclusivamente enlaces simples carbono-carbono. El nombre de parafinas (que hace referencia a su «pereza a reaccionar» [ parum : poco, affinis : afinidad], se dio inicialmente a estos compuestos al observar que prácticamente no reaccionaban con los reaccionantes más corrientes](https://image.slidesharecdn.com/tema10-110420024416-phpapp02/85/Tema-10-22-320.jpg)