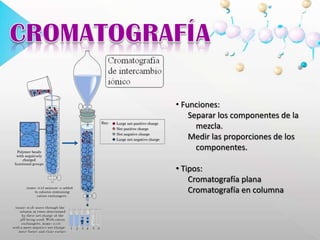
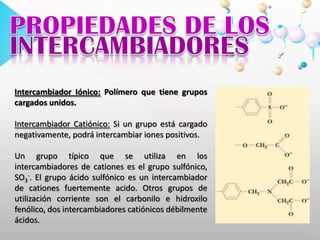
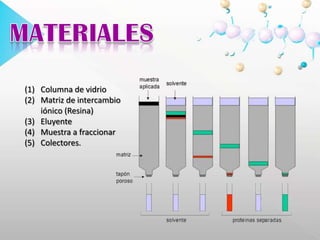
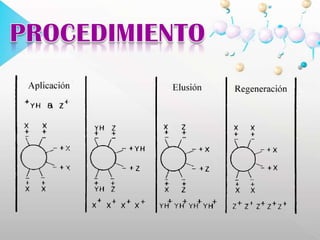
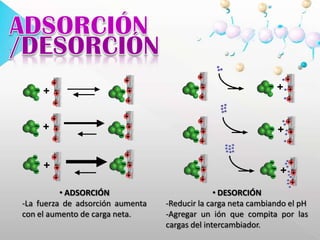
Este documento describe la cromatografía de intercambio iónico, un método de separación basado en las propiedades de carga de las moléculas. Se utiliza una fase estacionaria con cargas electrostáticas que retienen contraiones móviles que pueden intercambiarse por iones de la fase móvil. Se explican conceptos como adsorción, elución y aplicaciones como la medición de hemoglobina glicosilada y determinación de ácido delta-aminolevulínico y porfobilinógeno en orina.










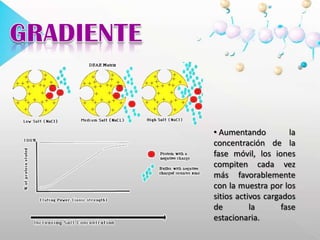
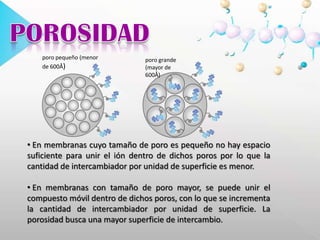
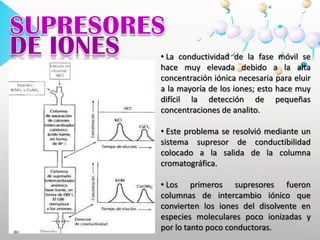
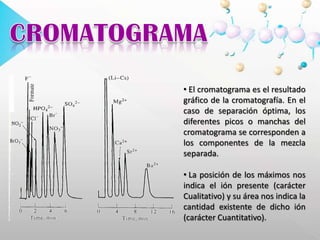



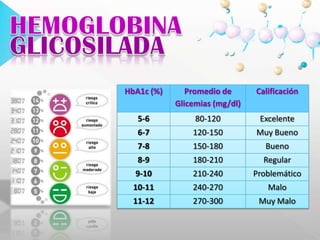
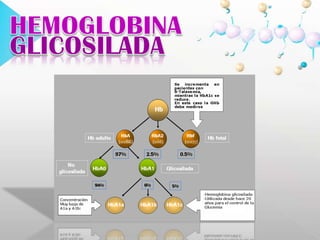
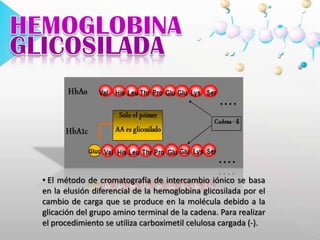
![HEMOGLOBINAGLICOSILADA El método de cromatografía de intercambio iónico se basa en la elusión diferencial de la hemoglobina glicosilada por el cambio de carga que se produce en la molécula debido a la glicación del grupo amino terminal de la cadena. Para realizar el procedimiento se utiliza carboximetil celulosa cargada (-).PBG Y ALAEN ORINAPorfirias: grupo de enfermedades de origen genético o adquirido. Existe alteración en la actividad de una o varias enzimas de la vía metabólica del grupo HEM, lo que ocasiona niveles anormalmente elevados de porfirinas o sus precursores (ácido delta-aminolevulínico [ALA] y porfobilinógeno [PBG]).](https://image.slidesharecdn.com/presentacion-100629224923-phpapp02/85/Cromatografia-de-intercambio-ionico-29-320.jpg)



