3826684.ppt
- 2. INTRODUCCION Los virus son parásitos intracelulares. Están constituidos por DNA o RNA de una sola o doble hebra envueltas por una cubierta proteica llamada cápside. Algunos poseen una cubierta lipídica que, en forma similar a la cápside, puede contener glicoproteínas antigénicas. La mayoría de los virus contienen enzimas, esenciales para su replicación o codifican éstas y usan la maquinaria del huésped para su síntesis. Los agentes antivirales efectivos actúan: inhibiendo eventos replicativos propios del virus, o inhibiendo la síntesis de ácidos nucleicos o proteínas en forma preferente sobre las de la célula huésped, o. afectando moléculas de la célula huésped esenciales para la replicación viral (terapias de corta duración). Aunque muchos compuestos exhiben actividad antiviral in vitro, la mayoría afecta alguna función de la célula huésped y producen toxicidades inaceptables.
- 3. Los antivirales efectivos generalmente tienen un espectro de acción reducido y su sitio de acción es una proteína viral específica implicadas en la síntesis de ácidos nucleicos virales (polimerasa o transcriptasa) o en el procesamiento de proteínas del virus (proteasa). La mutación de sólo un nucleótido produce sustituciones de aminoacidos críticos en una proteína diana resistencia. Los antivirales en uso inhiben la replicación activa, por lo que la replicación continúa una vez que cesa su administración esencial la respuesta inmune para recuperarse de la infección. Los fracasos clínicos de infecciones por virus sensibles pueden deberse a inmunosupresión severa o a la emergencia de variantes resistentes. La mayoría de los virus resistentes se aislan de pacientes inmunodeprimidos con alta carga replicativa viral y que han tenido tratamientos repetidos o prolongados (excepción: virus Influenza A). Los antivirales en uso NO eliminan virus latentes (en etapa no replicativa), aunque algunos antivirales son efectivos en suprimir en forma crónica la reactivación de la enfermedad..
- 4. La eficacia clínica depende de las concentraciones inhibitorias alcanzadas en el sitio de la infección, por ejemplo los análogos de nucleósidos deben entrar a la célula huésped y activarse por fosforilación intracelular. Para ello es crítico contar con las concentraciones necesarias de las enzimas que lo activan o de concentraciones adecuadas de los nucleótidos celulares con los cuales competirán esto afecta el efecto antiviral en células de distintos tipos y en diferente estado metabólico. Los tests de sensibilidad in vitro no están estandarizados, excepto para algunos virus (virus herpes simplex), y los resultados dependen del sistema de ensayo, tipo de célula, inóculo viral, y el laboratorio que lo realice para la mayoría de los virus no existe relación clara entre concentración activa antiviral con aquellas alcanzadas en sangre u otros fluidos y la respuesta clínica.
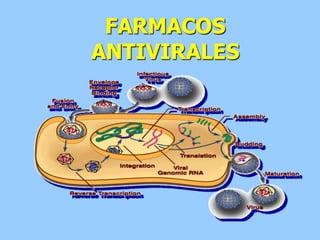
- 5. REPLICACIÓN VIRAL Absorción Entrada y denudamiento Síntesis de proteínas regulatorias temprana Síntesis de DNA o RNA Síntesis de proteínas estructurales Ensamblaje Liberación viral
- 6. Fármacos anti virus herpes: y citomegalovirus: Aciclovir IV, Oral, Tópico, Oftálmico Cidofovir IV Famciclovir Oral Foscarnet IV, Oral Fomivirsen Intravitreal Ganciclovir IV, Oral, intravitreal Idoxuridina Oftálmico Penciclovir IV Trifluridina Oftálmico Valaciclovir Oral Valganciclovir Oral Fármacos anti virus sincicial: Ribavirin Inhalado Fármacos anti influenza: Amantadine Oral Oseltamivir Oral Rimantadine Oral Zanamivir Inhalado Fármacos anti hepatitis: Adefovir Oral Lamivudine Oral Ribavirina Oral Interferon alfa Pegilado SC Fármacos anti VIH: INTR INNTR IP Inhibidores entrada
- 7. Mecanismos Generales Mecanismo Principales Fármacos Penetración y denudamiento Amantadina, Rimantadina DNA polimerasas virales Aciclovir, Foscarnet y Ganciclovir RNA polimerasas virales Foscarnet, Ribavirina Transcriptasa Reversa AZT, Didanosina, Zalcitabina, Estavudina, Nevirapina Aspartato Proteasa Indinavir, Ritonavir, Saquinavir, Nelfinavir Neuramidasa Viral Zanamivir, Oseltamivir
- 8. Las infecciones por virus herpes simplex tipo 1 (VHS-1) produce enfermedades de la boca, cara, piel, esófago y cerebro. El virus herpes simplex tipo 2 (VHS-2) generalmente produce infecciones de los genitales, recto, piel, manos y meninges. Ambos producen infecciones serias en neonatos. La vidarabina (1977) fue el primer antiviral aprobado para uso por vía sistémica en infecciones por VHS inhibe DNA polimerasas virales en mayor grado que las mamíferas. Debido a su toxicidad, su uso estaba restringido a infecciones fatales por VHS (encefalitis) y VZ (pacientes inmunodeprimidos). El aciclovir (1982) constituyó el primer antiviral efectivo para el tratamiento en pacientes ambulatorios de infecciones menos severas por VHS y VZ y inhibe DNA polimerasas virales pero no las mamíferas. Herpes Simplex y V. Zoster
- 9. Herpes Simplex y V. Zoster ACICLOVIR: Derivado cíclico de guanosina Mecanismo de acción Inhibición síntesis DNA por dos vías: - Aciclovir timidina quinasa viral 200 veces + afín por aciclovir aciclo GMP en células infectadas fosforilación por quinasas celulares aciclo GTP potente inh. DNA polimerasa viral pero no de la celular. - Aciclo GTP base anormal que se incorpora al DNA viral detención síntesis DNA viral. Oral (15-20% biodisponibilidad) y E.V. Resistencias: Timidina kinasa y DNA polimerasa Reacciones adversas: trastornos GI, nefropatía cristalina reversible
- 10. Mecanismo
- 11. Cont. VALACICLOVIR: L-valil ester del aciclovir aum. biodisp. oral aciclovir 3-5x Convertido rápidamente en aciclovir Primer episodio herpes genital Reduce la enfermedad por CMV en órganos trasplantados. PENCICLOVIR: Análogo de guanosina de uso tópico al 1% (baja biod. oral) FAMCICLOVIR: Prodroga: diacetil ester de 6-desoxipenciclovir Efecto primer paso: conversión a Penciclovir No produce terminación de la cadena y menor afininidad DNA polimerasa Efecto menos potente pero más prolongado que aciclovir 70% biodisponibilidad y menos de 20% unión a proteínas Efectos adversos: GI, toxicidad testicular
- 12. TRIFLURIDINA: Tópica 1%, 1a elección queratoconjuntivitis Nucleósido de pirimidinas fluorinado que inhibe la síntesis de DNA viral y en < grado la celular Infección en pctes resistentes a aciclovir HVS-1 y HVS-2, CMV, Vaccinia y algunos adenovirus FOSCARNET (VHS y VZ resist. a aciclovir; CMV resist. ganciclovir) Inhibe DNA polimerasa VHS o TR del VIH bloqueo no-competitivo unión de pirofosfato inhibe hidrólisis pirofosfato de deoxinucleótidos trifosforados. Inhibe 100 veces más la DNA polimerasa de VHS que las mamíferas. Baja biodisponibilidad oral ev. Depósito en huesos liberado lentamente. Nefrotoxicidad e hipocalcemia. Cont.
- 13. SNC (cefalea ~ 25 % pctes, temblor, irritabilidad, convulsiones y alucinaciones). Aumento o disminución en Ca2+ y fosfato, hipomagnesemia, e hipokalemia Rash generalizado, fiebre, náuseas o emesis, anemia, leucopenia, tests de función hepática anormales, cambios electrocardiográficos, tromboflebitis asociada a infusión y ulceraciones genitales dolorosas. Tópico irritación local y ulceración; oral alteraciones GI. Altas concentraciones mutagénicas y anormalidades esqueleto y dientes en fetos animales. No se conoce su seguridad en el embarazo o en niños. Cont.
- 14. Cont. Agente Vía Indicación Aciclovir Oral E.V. Primer episodio herpes simple genital Infección genital recurrente Infección mucocutánea en inmunosuprimidos Varicela y VZ Infección severa, encefalitis herpética, neonatal y v. zoster en inmunosuprimidos Famciclovir efecto + largo que aciclovir Valaciclovir > biodisp. que aciclovir Foscarnet E.V. Oral Oral Primer episodio herpes simple genital Infección genital recurente Supresión de herpes genital y VZ Primer episodio herpes simple genital Infección genital recurente Supresión de herpes genital y VZ Resistencia a aciclovir en HSV y VZV
- 15. CITOMEGALOVIRUS GANCICLOVIR: Análogo acíclo de guanosina Idem aciclovir, pero fosforilación a ganciclo GMP catalizado por quinasas virales y celularesganciclo GTP inhib DNA polimerasa viral Oral, e.v., implante intraocular Retinitis por CMV y profilaxis (oral) Mielo supresión: neutropenia 20-40% de los pctes VALGANCICLOVIR: Ester monovalil que funciona como profármaco de ganciclovir Inducción y mantenimiento en renitinitis por CMV
- 16. Cont. CIDOFOVIR: Análogo nucleótido de citosina Inhibe síntesis DNA viral por término de la elongación de la cadena. Quinasas celulares difosfato inh. competitivo de dCTP y se incorpora como base anormal al DNA viral. Conc. inhib. DNA polimerasa viral son 1/8 a 1/600 la conc. necesaria para inhibir polimerasa celular. T1/2: 2.6 hora, metabolito difosfato incrementa biodisp. intracel 17-65 horas VHS y CMV, ev para inducción y mantenimiento FOMIVIRSEN: Oligonucleótido unión a mRNA diana inh. síntesis proteica temprana inh. replicación Resistencia cruzada con ganciclovir, foscarnet Intravitreal para retinitis por CMV en pctes. con HIV Utilizado cuando hay intolerancia a otras drogas Efectos adversos: iritis y vitreitis, aumento presión intraoc.
- 17. El tropismo del VIH está controlado por la proteína de cubierta gp160. El sitio diana de unión de gp160 es el receptor CD4 en linfocitos y macrófagos. La entrada a la célula requiere también la unión a un co-receptor quemoquina CCR5 o CXCR4. La mayoría de los indiv. infectados tienen virus con tropismo por CCR5; el CCR5 está presente en macrófagos. Se cree que el virus CCR5 es el que produce la transmisión sexual y que este co-receptor se expresa en las células inicialmente infectadas Un cambio del uso por el virus del CCR5 por CXCR4 se asocia a progresión de la enfermedad, e infección de linfocitos T. El cambio fenotípico de CCR5 a CXCR4 pronostica pérdida acelerada de células CD4+ helper T y el aumento de riesgo de inmunosupresión. No se sabe si este cambio en co-receptor es la causa o el producto de la progresión de la enfermedad. Virus de la Inmunodeficiencia Humana
- 18. La región gp41 de la cubierta controla la fusión de la capa de lípidos con la de la célula huésped entrada RNA al citoplasma replicación a un complejo RNA-DNA DNA doble hebra por transcriptasa reversa (TR). La TR tiende a producir errores y no tiene una función que asegure una buena lectura mutaciones frecuentes. El DNA viral es transportado al núcleo donde se integra al cromosoma celular por la integrasa viral en un lugar al azar. Luego de la integración, el virus puede permanecer en estado latente y replicarse cuando la célula se divide. Las proteínas transmembranas y estructurales se ensamblan alrededor del RNA y forman la nucleocápside; este provirus se ensambla cerca de la membrana celular en lugares ricos en colesterol. “Brotan” a través de la membrana celular; la TR se incorpora a esta partícula y el virus “madura” a través de hidrólisis catalizadas por una aspartil proteasa forma madura infectante .
- 19. Virus de la Inmunodeficiencia Humana (VIH-1 y VIH-2)
- 20. PUNTOS DE ATAQUE AL VIH: FUSION TRANSCRIPTASA REVERSA: MUY CAMBIANTE! Es posible que en un día se produzcan todas las mutaciones posibles de todos los nucleótidos INTEGRASA S-1360 (en desarrollo) ASPARTIL PROTEASA 3 genes mayores muy similares para ambos (Gag-Pol y Env) aunque inhibidores no nucleosídicos de transcriptasa reversa no son activos frente a VIH-2 Poliproteína Gag-Pol debe ser desdoblada por la proteasa, sino son viriones inmaduros o no infectantes.
- 21. • Inhibidores de la Transcriptasa reversa: INH. NUCLEOSÍDICOS (INTR): ZIDOVUDINA (AZT), (1987) DIDANOSINA (ddA) ESTAVUDINA (d4T) ZALCITABINA (ddC) LAMIVUDINA (3TC) INH. NO NUCLEOSÍDICOS (INNTR): NEVIRAPINA (NVP) (1998) EFAVIRENZ (EFV) FOSCARNET DELAVIRDINA (DLV) • Inhibidores de la Proteasa de HIV (IP): (1995) SAQUINAVIR (SQV), RITONAVIR (RTV), INDINAVIR (IDV), NELFINAVIR (NFV), AMPRENAVIR (APV), ATAZANAVIR (ATV), LOPINAVIR (LPV) • Inhibidores de la entrada viral: (2003)
- 22. Son fosforilados por enzimas del citoplasma de la célula huésped a nucleósidos trifosforados inhibición competitiva de DNA polimerasa inversa. Carecen del 3’-OH : se incorporan al ADN y “cortan” el crecimiento de la cadena Pueden entrar a la célula por difusión pasiva o por un transportador de nucleobases (según el compuesto) Activos contra VIH-1 y VIH-2 INTR: MECANISMO DE ACCIÓN
- 23. REACCIONES ADVERSAS INTR ZIDOVUDINA (AZT): Azidotimidina inhibe la TR por competencia entre los nucleótidos Terminación de la cadena en el DNA viral Resistencia por mutación Biodisponibilidad 60-65% V.O., biodisp. con: antimicóticos, cimetidina, dometacina, TMX-SMX; con rifampicina Efectos adversos: Hematoxicidad, cefaleas, astenia, mialgias, miopatías
- 24. OTROS INTR: Didanosina (DDI): pancreatitis y neuropatía periférica Zalcitabina (DDC): neuropatía periférica, distrés GI, neutropenia Estavudina (D4T): neuropatía periférica Lamivudina (3TC): GI, cefalea Tenofovir (TDF): GI, renal Cont.
- 25. Compuestos sintéticos de muy distinta estructura química No son fosforilados Se unen a una región hidrófoba de la DNA polimerasa inversa, distinta del sitio catalítico e inducen cambios constitutivos en la misma Sólo actúan frente a HIV-1 Son metabolizados por el CYP450 conllevando interacciones medicamentosas Generalmente penetran a la célula por difusión Originan rápida resistencia por mutaciones, especialmente en el codón 103 y también en el 181 INNTR: MECANISMO DE ACCIÓN
- 26. REACCIONES ADVERSAS INNTR NEVIRAPINA: Rash, hepatotoxicidad EFAVIRENZ: SNC (vértigo, psicosis), rash, hepatotoxicidad, dislipidemia, potencialmente teratogénico
- 27. INHIBIDORES DE LA PROTEASA DE HIV (resistencia de aparición lenta) Diseñados a partir del conocimiento de la estructura tridimensional de la enzima y sustrato y otros inhibidores No interfieren con proteasas humanas La afinidad de los inhibidores de proteasas de HIV es 1000 veces superior para esta que para las proteasas del individuo Inhibidores competitivos: unión reversible Proteasa: desdobla la poliproteína GAG-POL del lado del N terminal de residuos prolina Enzimas: TR, PR, integrasa GAG-POL Proteínas estructurales: p17, p24, p9, p7 Concentraciones subóptimas favorecen la resistencia
- 28. Resistencia: mutación de Pol. Reacciones adversas: náuseas, vómitos, diarrea y parestesia Otras: Indinavir: Principal nefrolitiasis (hidratar). Menor frec. redistribución grasa, pérdida cabello, piel seca, insomnio, cefalea Nelfinavir: Diabetes, intolerancia a la glucosa, colesterol y triglicéridos Ritonavir: colesterol y triglicéridos Amprenavir: Hiperglicemia, fatiga, cefalea Lopinavir: colesterol y triglicéridos Cont.
- 29. Cont. Interacciones Todos los IP son sustratos e inhibidores de la isoforma CYP3A4 de la enzima Citocromo P450 interacciones son comunes. Potencia de inhibición CYP3A4: ritonavir >>(indinavir, amprenavir, nelfinavir) > saquinavir ritonavir dosis bajas efectos otros IP clearance de deriv. ergot, cisaprida, triazolam, midazolam. Rifampicina clearance IP Ritonavir: induce CYP 1A2, aumenta el efecto de eritromicina, ketoconazol y rifampicina
- 30. INHIBIDORES ENTRADA VIH Enfuvirtida Péptido sintético derivado de región transmembrana gp41 del VIH-1. No es activa contra VIH-2. Inhibe selectivamente fusión de la membrana celular inducida por el VIH. Cara y se debe administrar 2 veces al día por vía sc., lo que limita su uso reservado a pacientes en que otras terapias han fracasado. Mecanismo de acción único activa contra virus resistentes a otros anti retrovirales. Resistencia por mutaciones específicas en el sitio gp41 resistencia clínica requiere 2 o más cambios de aminoacidos en región gp41 Reacción en sitio de inyección: dolor, eritema e induración; el 98% de los pacientes desarrollan nódulos o quistes en el sitio de la inyección. Su uso se ha asociado con un aumento de linfoadenopatías y neumonia
- 31. Tratamiento antiretroviral (TAR) en Chile En pacientes con infección crónica VIH que presentan algunas de las siguientes situaciones: Antecedente de enfermedad oportunista de etapa C (excepto TBC) Recuento CD4 < 200 céls/mm3; recuento CD4 entre 200-250 céls/mm3 con carga viral (CV) > 100.000 copias/mL; Candidiasis orofaríngea; diarrea crónica; fiebre prolongada o baja de peso. La TAR con 3 antivirales constituye el estándar de manejo para niños y adultos infectados crónicamente con VIH. Modelos matemáticos de la replicación del VIH sugieren que se requiere un mínimo de 3 agentes para garantizar supresión a largo plazo de la replicación del VIH sin resistencia. Las combinaciones con la que existe mayor experiencia clínica son: 2 INTR + 1 INNTR 2 INTR + 1 IP reforzado (adición Ritonavir dosis baja para Cp) 3 INTR 1 INTR + 1 INNTR + 1 IP (niños)
- 32. TAR: Esquema de 1a línea 2 INTR + 1 INNTR 2 INTR + 1 IP reforzado Por razones de potencia equivalente, simplicidad de adm., y menor incidencia de reacciones adversas de largo plazo: Zidovudina / Lamivudina coformulados + Efavirenz Si hay contraindicación para AZT (anemia, neutropenia, quimioterapia por tox. hematológica AZT ) reemplazar por didanosina (ddI) Si hay contraindicación para Efavirenz (patología psiquiátrica por tox. SNC; mujeres edad fértil por potenciales efectos teratogénicos) reemplazar por Nevirapina En pacientes con Sarcoma de Kaposi agresivo se recomienda Zidovudina + Lamivudina + coformulación Lopinavir/Ritonavir por efecto específico de IP en la angiogénesis del Sarcoma de Kaposi
- 33. PROFILAXIS VIH Contacto directo (sangre, semen y otras secreciones sexuales) Preservativos disminuyen marcadamente la probabilidad de contraer VIH y hepatitis B Transmisión Vertical El VIH puede transmitirse desde la madre infectada al feto por la placenta y al recién nacido a través de la leche materna 90 % responsable de los casos de SIDA infantil TAR a partir de la semana 24 de gestación con: Zidovudina - Lamivudina - Nelfinavir o Zidovudina - Lamivudina - Saquinavir/Ritonavir Cesárea electiva a las 38 semanas de gestación, antes de una eventual rotura de membranas o del inicio de parto espontáneo.
- 34. AZT e.v. continuo a la madre desde 4 h antes del parto o cesárea hasta el alumbramiento o AZT - Lamivudina oral AZT en jarabe o inyectable a partir 8-12 h y durante las primeras 6 semanas de vida en todos los RN RN cuyas madres no recibieron TAR AZT + Nevirapina transmisión vertical en un 80 % Nevirapina: 1 dosis al inicio del parto y otra al neonato transmisión vertical en 50-87% Suspensión completa lactancia materna Cont.
- 35. Fármacos anti influenza AMANTADINA y RIMANTADINA: Bloquean denudamiento y ensamblaje virus influenza A Uso profiláctico principalmente; eficacia: 50-90% (similar vacuna) Disminuye los efectos de la gripe en 1-2 días Livedo reticularis, ICC, insomnio y convulsiones, menos frec. con rimantadina ZANAMIVIR Y OSELTAMIVIR: Utilidad contra Influenza A y B resist. a amantadina Inhib. neuraminidasas agreg. viral en la superficie celular disminuye propagación virus dentro del tracto respiratorio. Profilaxis y reducen síntomas de gripe en 2-3 días Náuseas y vómitos (zanamivir inhalado), irritación naríz y garganta RIBAVIRINA aerosol (Virus sincicial respiratorio, Infl A y B) : Inhibe inosina 5 P deshidrogenasa e interfiete con síntesis de GTP. Anemia por hemólisis extravascular, depresión de la médula ósea; elevación de bilirrubina, fierro y ácido úrico. Terapia oral prolongada síntomas GI y del SNC
- 36. Fármacos anti hepatitis crónicas B y C Adefovir (VHB) Deriv. difosfato inh. comp. de deoxiadenosina trifosfato inh. la DNA polimerasa viral y transcriptasa reversa y tb. finaliza la cadena de la síntesis de DNA viral Nefrotoxicidad y disfunción tubular (azotemia, hipofosfatemia, acidosis, glicosuria y proteinuria) gral. reversible meses después de discontinuado. Ribavirina oral + Interferón im o sc (VHC) Lamivudina (VHB)
- 37. FIN