Colageno 1
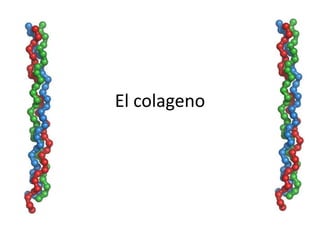
- 1. El colageno
- 2. EL COLÁGENO ESTRUCTURA: El colágeno es una proteína constituyente de los tejidos conjuntivos, como: la piel, los tendones y el hueso. Es la proteína más abundante del organismo, se caracteriza principalmente por su resistencia y está constituido por tres cadenas polipeptídicas (1000 aminoácidos por cadena). Su solidez se ve asegurada por enlaces transversales entre las cadenas polipetídicas..
- 3. Fibras de colageno. Son las más abundantes de los tejidos conjuntivos y están constituidas por una proteína fibrilar: la colágena, denominada así porque se hidrata ante la cocción y se transforma en gelatina (cola). Se conocen también como “fibras blancas”, porque tienen ese color en estado fresco, sobre todo en órganos como tendones o aponeurosis, que están formados principalmente por este tipo de fibra.
- 4. Morfología: Son largas y de forma cintada. En un corte transversal tienen forma elíptica. Se disponen en haces ondulados que forman espirales que varían en los tejidos. Su diámetro está entre 1-12 μm. Propiedades físicas: Son birrefringentes y anisótropas. Aplicándoles luz polarizada aparecen dotadas de birrefringencia uniáxica positiva, lo que indica una orientación longitudinal de las fibrillas. Propiedades químicas: El agua a temperatura de ebullición transforma las fibras colágenas en una masa viscosa que se convierte en gelatina. Los ácidos y los álcalis débiles las disuelven pues las tornan hidrófilas. Son digeridas por colagenasa y pepsina en solución ácida, pero resisten a la tripsina. Cuando se trata con sales de metales pesados, forman un producto insoluble.
- 8. BIOSÍNTESIS: Antes de llegar a su estructura definitiva, la molécula de colágenos experimenta una serie de modificaciones. • La lectura del ARNm constituye la fase inicial de la biosíntesis. • Los polisomas ensamblan los aminoácidos para formar las cadenas polipeptídicas. • Las cadenas polipeptídicas (cadenas proalfa) llevan en sus extremos secuencias suplementarias de aminoácidos. • Las cadenas proalfa sufren hidroxilación, los grupos peptidil-prolina se transforman en hidroxi-prolina y los grupos peptidil-lisina se convierte en hidroxi-lisina. • En los grupos hidroxi-lisina se fijan moléculas de galactosa y glucosa, y en los grupos terminales se fijan otros azúcares. • Se crean puentes disulfuro (S-S) entre las cadenas polipeptídicas. • Se forma la molécula de procolágeno.
- 9. Molécula de Procolágeno: •Transita por las vesículas de Golgi pasando al medio extracelular. •Bajo la acción de las proteasas sufre una escisión de los grupos N-terminal y C- terminal. •Luego las moléculas de colágeno se constituyen en fibras.
- 10. IMPORTANCIA: El colágeno sufre una serie de alteraciones en su estructura molecular, colagenosis. Y el conjunto de varias de estas alteraciones se denominan conectivitis. En 1942, Klemperer y colaboradores, englobaron diferentes afecciones diseminadas de colagenosis, como: la degeneración fibrinoide, que secaracteriza por la anomalía en la estructura y metabolismo del colágeno.
- 11. ENFERMEDADES DEL COLÁGENO: Se clasifican por distintos síntomas:
- 12. Síndrome de Ehlers-Danlos Hiper elasticidad cutánea y una hiperlaxitud ligamentaria. Se encuentra en las de tipo: IV, V, VI, VII.
- 13. Dermatosparaxis •Se da en ovinos o bovinos. •Su colágeno esta constituido por cadenas proalfa. •Las fibras son frágiles e irregulares. •Los animales mueren de inmediato por desgarres cutáneos (provocados por traumatismos).
- 14. Osteogénesis Imperfecta •Déficit de la síntesis de colágeno. •Presenta fragilidad ósea e hiperlaxitud cutánea y articular.
- 15. Enfermedad de Marfán •Anomalía en los enlaces transversales de la molécula de colágeno. •Longitud excesiva de los miembros, hiperlaxitud ligamentosa, escoliosis y tórax en embudo. •Malformaciones cardiovasculares.
- 16. Escorbuto •Déficit de ácido ascórbico (interviene en las reacciones enzimáticas). •Altera la síntesis de fibras de colágeno.
- 17. Esclerodermia •Trastorno grave de colágeno o Acumulación de colágeno en los tejidos. •Aceleración de síntesis de colágeno.
- 18. CRISTALIZACIÓN Y DEPÓSITO DE COLÁGENO Una lesión tisular se sigue de un proceso de reparación, que incluye: En los animales: Invasión de la zona lesionada por los fibroblastos y luego un depósito de colágeno. En el hombre: Formación de cicatrices y fibrosis permanentes. Constitución de una reacción fibrosa.