Clase 4 Tendencias PerióDicas
•Descargar como PPT, PDF•
2 recomendaciones•12,136 vistas
Denunciar
Compartir
Denunciar
Compartir
Más contenido relacionado
La actualidad más candente
La actualidad más candente (20)
Similar a Clase 4 Tendencias PerióDicas
Similar a Clase 4 Tendencias PerióDicas (20)
Propiedades de la tabla periódica, configuración electrónica.pdf

Propiedades de la tabla periódica, configuración electrónica.pdf
Propiedades periódicas de los elementos químicos (2).pdf

Propiedades periódicas de los elementos químicos (2).pdf
Estructura electronica de los atomos y la ley periodica

Estructura electronica de los atomos y la ley periodica
Propiedades periódicas de los elementos químicos (2).pptx

Propiedades periódicas de los elementos químicos (2).pptx
Más de lucas crotti
Más de lucas crotti (20)
Último
Último (20)
u1_s4_gt_la demanda y la oferta global_b27t9rulx9 (1).pptx

u1_s4_gt_la demanda y la oferta global_b27t9rulx9 (1).pptx
Rendicion de cuentas del Administrador de Condominios

Rendicion de cuentas del Administrador de Condominios
Proyecto TRIBUTACION APLICADA-1.pdf impuestos nacionales

Proyecto TRIBUTACION APLICADA-1.pdf impuestos nacionales
Habilidades de un ejecutivo y sus caracteristicas.pptx

Habilidades de un ejecutivo y sus caracteristicas.pptx
El MCP abre convocatoria de Monitoreo Estratégico y apoyo técnico

El MCP abre convocatoria de Monitoreo Estratégico y apoyo técnico
20240418-CambraSabadell-SesInf-AdopTecnologica-CasoPractico.pdf

20240418-CambraSabadell-SesInf-AdopTecnologica-CasoPractico.pdf
Mapa Conceptual relacionado con la Gerencia Industrial, su ámbito de aplicaci...

Mapa Conceptual relacionado con la Gerencia Industrial, su ámbito de aplicaci...
Clase 4 Tendencias PerióDicas
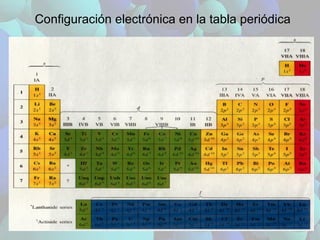
- 1. Configuración electrónica en la tabla periódica
- 3. Volviendo a la tabla periódica….. Elementos con configuración electrónica similar tienen propiedades similares (grupos – columnas) La tabla periódica se ordena por masa atómica creciente (número de protones y número de electrones) lo que lleva al incremento de electrones de valencia (filas horizontales de la tabla) Los elementos de los grupos principales n = 2 completan los orbitales s y p. Los elementos de transición tienen n = 3, se completan orbitales s, p y d.
- 6. Radio Atómico Decrece de izquierda a derecha dentro del período debido a la mayor carga nuclear efectiva Se incrementa hacia abajo dentro del grupo debido al mayor tamaño de los orbitales con mayor n
- 14. Tendencia Periódica - EI La energía de ionización crece con el período de izq. a derecha La energía de ionización decrece con el grupo hacia abajo
- 15. EI sucesivas
- 16. Afinidad Electrónica (AE): es la energía involucrada en la aceptación de un electrón. Puede ser positiva o negativa: a mayor valor positivo, presenta mayor tendencia a aceptar un electrón, los valores negativos indican poca tendencia del elemento a aceptar un electrón. Atomo + Electrón átomo (anión) + AE
- 17. Tendencias en Afinidad Electronica
- 18. Resumen de las tendencias
- 19. Entendiendo un grupo Grupo 1A: Metales Alcalinos
- 20. La Hélice “Telúrica” (1862)
- 21. Las “octavas” de Newland (1865)
- 22. La tabla periódica de Bayley – Thomsen - Bohr
- 23. La Tabla periódica de Alexander
