Resumen 1ra ley termodinamica y ejercicios (1).pptx
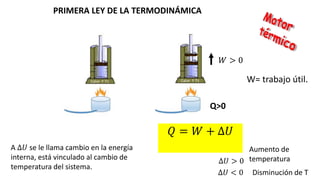
- 1. Q>0 𝑊 > 0 PRIMERA LEY DE LA TERMODINÁMICA 𝑄 = 𝑊 + ∆𝑈 A ∆𝑈 se le llama cambio en la energía interna, está vinculado al cambio de temperatura del sistema. ∆𝑈 > 0 ∆𝑈 < 0 Aumento de temperatura Disminución de T W= trabajo útil.
- 2. TRABAJO DE EXPANSION EN LOS CAMBIOS DE VOLUMEN dx V1 V2 P NOTA : UN GAS EN EXPANSIÓN REALIZA TRABAJO POSITIVO
- 3. En general en la expansión la presión se reduce, por lo que tenemos: V1 V2 DIAGRAMAS P – V =Área bajo la curva
- 4. DIAGRAMA P-V GENERAL El trabajo en la trayectoria 12 es a presión contante. En la ruta 23 no hay trabajo externo pues es a volumen constante. 1 2 3 4 P1 P2 V1 V2
- 5. 1 2 3 4 P1 P2 V1 V2 Para cualquier ruta de realización del trabajo el cambio de energía interna es la misma. Por ejemplo para la ruta 1- 3 el cambio de energía será la misma que para la ruta 1-4-3- o 1-2-3 ∆𝑈13 = ∆𝑈143 = ∆𝑈123
- 6. CASO CUANDO EL SISTEMA NO GANA NI PIERDE CALOR (PROCESO ADIABATICO) ( Q =0) Ejemplo: P Se comprime lentamente tal que no se incremente el calor ni entre en ella Pared adiabática que no permite que el calor se transfiera al exterior o ingrese al recipiente Al comprimirse W<0, por tanto se incrementa la energía interna y aumenta la temperatura. Y en la expansión la energía interna disminuye y por tanto la temperatura.
- 7. CASO CUANDO NO HAY CAMBIO DE VOLUMEN (PROCESO ISOCORO) (W=0) P2 V V P1 Aplicando la primera ley de la termodinámica: Esto significa que todo el calor suministrado va al cambio de energía interna y por tanto de aumento de temperatura, si fuese disminución de presión esto provoca disminución de la temperatura.
- 8. CASO A TEMPERATURA CONSTANTE (PROCESO ISOTERMICO) (T es constante) Para un gas ideal: PV = nRT Esto se logra con cambio en presión y volumen muy lentamente Por la primera ley de la termodinámica: Esto significaría, por ejemplo, que todo el calor suministrado se convierte en trabajo externo.
- 9. P V V1 V2 Esto representa el área debajo de la línea que corresponde a P. CASO A PRESION CONSTANTE (PROCESO ISOBARICO) (presión = constante) Aplicando la primera ley de la termodinámica:
- 10. PROBLEMA En un sistema se realiza un cambio de estado de 𝑎 hasta 𝑏 a lo largo de la trayectoria 𝑎𝑐𝑏 durante este proceso ingresa al sistema 100 𝑘𝐽 de calor efectuando trabajo de 30 𝑘𝐽. Determine la cantidad de calor que ingresa al sistema a lo largo de 𝑎𝑑𝑏 si el trabajo realizado es 10 𝑘𝐽. DATOS: Qacb= +100 kJ Wacb= + 30 kJ Hallar Qadb =? ESTRATEGIA La fórmula que vamos a usar mayormente es 𝑸 = 𝑾 + ∆𝑼. Con dos datos obtenemos el tercero. (1 LTD) 1ro. Observamos que en la ruta acb hay dos datos, lo cual indica que podemos hallar el cambio de energía interna. El cambio de energía interna calculado es para acb, luego es también para adb. 2do. Con esto último hacemos uso nuevamente de la 1 LTD pero aplicado a adb. Wadb= + 10 kJ
- 11. DATOS: Qacb= +100 kJ Wacb= + 30 kJ Hallar Qadb =? Wadb= + 10 kJ 1ro. Usamos la 1LTD en la ruta acb 𝑄 = 𝑊 + ∆𝑈 𝑄𝑎𝑐𝑏 = 𝑊𝑎𝑐𝑏 + ∆𝑈𝑎𝑐𝑏 100 kJ = 30 𝑘𝐽 + ∆𝑈𝑎𝑐𝑏 ∆𝑈𝑎𝑐𝑏= 70 𝑘𝐽 Por tanto: ∆𝑈𝑎𝑑𝑏= 70 𝑘𝐽 ∆𝑈𝑎𝑐𝑏= ∆𝑈𝑎𝑏= ∆𝑈𝑎𝑑𝑏 2do. Usamos ahora la 1LTD en la ruta adb 𝑄 = 𝑊 + ∆𝑈 𝑄𝑎𝑑𝑏 = 𝑊𝑎𝑑𝑏 + ∆𝑈𝑎𝑑𝑏 𝑄𝑎𝑑𝑏 = 10 𝑘𝐽 + 70 𝑘𝐽 = 𝟖𝟎 𝒌𝑱
- 12. PROBLEMA MODELO DE CALCULO DE ENERGÍA, CALOR Y TRABAJO EN UN PROCESO TERMODINAMICO EMPLEANDO LA PRIMERA LEY DE TERMODINÁMICA (1LTD) Un proceso termodinámico es representado por un diagrama P-V, como se muestra, en el proceso ab se suministran al sistema 600 J de calor, y en el bd, 200 J. Calcular: a) El cambio de energía interna en el proceso ab. b) El cambio de energía interna en el proceso abd. c) El calor total suministrado en el proceso acd d) ¿En ab existe incremento de temperatura? ¿Por qué? e) ¿En qué procesos no se realiza trabajo? V (m3) 8 x 104 Pa 3 x 104 Pa 2x10-3 5x10-3 a b d c
- 13. a)El cambio de energía interna en el proceso ab. V (m3) 8 x 104 Pa 3 x 104 Pa 2x10-3 5x10-3 a b d c DATOS: Qab= +600 J Qbd= +200 J Para todos los casos usaremos: 𝑄 = 𝑊 + ∆𝑈 Por tanto en ab: 𝑄𝑎𝑏 = 𝑊𝑎𝑏 + ∆𝑈𝑎𝑏 Donde: 𝑊𝑎𝑏 = 0 𝑄𝑎𝑏 = 0 + ∆𝑈𝑎𝑏 600 = 0 + ∆𝑈𝑎𝑏 600 = ∆𝑈𝑎𝑏 ∆𝑼𝒂𝒃= 𝟔𝟎𝟎 𝑱 Como este cambio de energía interna es positivo, se deduce que hay aumento de temperatura en el sistema.
- 14. b) El cambio de energía interna en el proceso abd. DATOS: Qab= +600 J Qbd= +200 J V (m3) 8 x 104 Pa 3 x 104 Pa 2x10-3 5x10-3 a b d c Para todos los casos usaremos: 𝑄 = 𝑊 + ∆𝑈 Por tanto en abd: 𝑄𝑎𝑏𝑑 = 𝑊𝑎𝑏𝑑 + ∆𝑈𝑎𝑏𝑑 𝑊𝑎𝑏𝑑 = 𝑊𝑎𝑏 + 𝑊𝑏𝑑 𝑊𝑎𝑏𝑑 = 𝑊𝑏𝑑 = 8 𝑥 104 (5𝑥10−3 − 2𝑥10−3 ) = 240 𝐽 𝑄𝑎𝑏𝑑 = 𝑄𝑎𝑏 + 𝑄𝑏𝑑 = 𝟔𝟎𝟎 + 𝟐𝟎𝟎 = 𝟖𝟎𝟎 𝑱 Por tanto en abd: 𝑄𝑎𝑏𝑑 = 𝑊𝑎𝑏𝑑 + ∆𝑈𝑎𝑏𝑑 𝑄𝑎𝑏𝑑 = 𝑊𝑎𝑏𝑑 + ∆𝑈𝑎𝑏𝑑 800 = 240 + ∆𝑈𝑎𝑏𝑑 ∆𝑼𝒂𝒃𝒅= 𝟓𝟔𝟎 𝑱
- 15. c) El calor total suministrado en el proceso acd. DATOS: Qab= +600 J Qbd= +200 J V (m3) 8 x 104 Pa 3 x 104 Pa 2x10-3 5x10-3 a b d c Para todos los casos usaremos: 𝑄 = 𝑊 + ∆𝑈 Por tanto en acd: 𝑄𝑎𝑐𝑑 = 𝑊𝑎𝑐𝑑 + ∆𝑈𝑎𝑐𝑑 𝑊𝑎𝑐𝑑 = 𝑊 𝑎𝑐 + 𝑊𝑐𝑑 𝑊𝑎𝑐𝑑 = 𝑊 𝑎𝑐 = 3 𝑥 104 (5𝑥10−3 − 2𝑥10−3 ) = 90 𝐽 Como: ∆𝑈𝑎𝑏𝑑 = ∆𝑈𝑎𝑐𝑑 = 560 𝐽 Por tanto: 𝑄𝑎𝑐𝑑 = 𝑊𝑎𝑐𝑑 + ∆𝑈𝑎𝑐𝑑 𝑄𝑎𝑐𝑑 = 90 + 560 𝑄𝑎𝑐𝑑 = 650 𝐽
- 16. PROBLEMA El ciclo lo realiza un gas ideal, en el punto A la temperatura es de 700 𝐾, la presión 20 𝑏𝑎𝑟 y el volumen 2 𝐿. En el punto B el volumen es de 5 𝐿. Si 𝑘 = 1.5. a) ¿Cuál de los procesos es adiabático y cual isotérmico? b) Hallar la presión en B y C. c) Hallar el trabajo B-C. SOLUCION En el punto A: TA= 700 K PA= 20 bar VA= 2 L En el punto B: TB= ? PB= ? VB= 5 L k=1.5 ESTRATEGIA Para la parte a) Identificamos que CA es isotérmica (comparar con gráfico de la teoría) y AB es adiabático Para la parte b) PB=PC, usaremos para ello la ecuación para la adiabática en AB: PAVA k=PBVB k Para la parte c) simplemente usamos la fórmula del trabajo para un proceso isobárico: W=P(VC-VB) y detalles añadidos en la resolución
- 17. En el punto A: TA= 700 K PA= 20 bar VA= 2 L En el punto B: TA= ? PB= ? VB= 5 L k=1.5 b) Hallar PB y PC Usamos: 𝑃𝐴𝑉𝐴 𝑘 = 𝑃𝐵𝑉𝐵 𝑘 Reemplazamos: 20 𝑏𝑎𝑟 2 𝐿 1.5 = 𝑃𝐵(5 𝐿)1.5 𝑃𝐵 = (20 𝑏𝑎𝑟)( 2 5 )1.5 = 𝟓. 𝟎𝟓𝟗𝟔 𝒃𝒂𝒓 = 𝑷𝑪
- 18. En el punto A: TA= 700 K PA= 20 bar VA= 2 L En el punto B: TA= ? PB= ? VB= 5 L k=1.5 b) Hallar el trabajo en BC Para hacer uso de la fórmula 𝑊 = 𝑝(𝑉𝐶 − 𝑉𝐵) P lo conocemos, P= 5.0596 bar Sabemos que VB= 5 L y nos falta conocer VC Lo hallaremos usando la ecuación de gases ideales en la curva CA que es isotérmica. 𝑷𝑨𝑽𝑨 𝑻𝑨 = 𝑷𝑪𝑽𝑪 𝑻𝑪 Como TA=TC 𝑃𝐴𝑉𝐴 = 𝑃𝐶𝑉𝐶 (20 𝑏𝑎𝑟)(2 𝐿) = (5.0596 𝑏𝑎𝑟)𝑉𝐶 𝑉𝐶 = 7.905763 𝐿 Ahora sí, ya podemos: 𝑊 = 𝑝(𝑉𝐶 − 𝑉𝐵) 𝑊 = 5.0596 𝑏𝑎𝑟 (7.905763𝐿 − 5𝐿) 𝑊 = 14.7020 𝑏𝑎𝑟. 𝐿 𝑥 𝟏𝟎𝟎 𝟎𝟎𝟎 𝑷𝒂 𝟏 𝒃𝒂𝒓 𝒙 𝟏 𝒎𝟑 𝟏𝟎𝟎𝟎 𝑳 𝑾 = 𝟏𝟒𝟕𝟎. 𝟐𝟎 𝑱