Enlaces quimicos
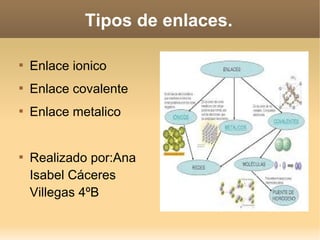
- 1. Tipos de enlaces. Enlace ionico Enlace covalente Enlace metalico Realizado por:Ana Isabel Cáceres Villegas 4ºB
- 2. Enlace ionico Se produce cuando los átomos de los elementos metálicos (los situados mas a la izquierda de la tabla periodica),se encuentran con átomos no metálicos(situados a la derecha).En este caso los átomos ceden electrones a los átomos del no metal,transformandose en iones positivos (cationes) y negativos (aniones)
- 3. Enlace covalente Este enlace se produce entre los átomos de los elementos no metálicos (los situados más a la tabla períodica).En este caso la tendencia a captar electrones es semejante entre los átomos. Los electrones se compartirán entre los átomos para quedar rodeados por 8 electrones (regla del octeto).
- 4. Enlaces metalico Este enlace se produce entre los átomos de los elementos metálicos (los situados en la parte izquierda de la tabla periódica).En este caso la tendencia a ceder electrones es semejante entre los átomos. Los electrones del último nivel (llamados electrones de valencia) se compartirán entre todos los átomos constituyendo lo que se llama nube o mar de electrones. Debido a esto, los metales son buenos conductores de la electricidad.Los restos iónicos (con carga positiva) se ordenan en una red tridimensional formando un cristal metálico